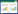2. 临沂市肿瘤医院妇科, 临沂 276000;
3. 临沂市人民医院病理诊断科,临沂 276000
2. Department of Gynecology, Linyi Cancer Hospital, Linyi 276000, China;
3. Pathology Diagnosis Department, Linyi People's Hospital, Linyi 276000, China
静脉-动脉体外膜肺氧合(veno-arterial extracorporeal membrane oxygenation V-A ECMO)作为一种体外生命支持技术近些年来发展迅猛,其应用率已呈指数增长[1]。然而,股动脉插管常可能导致同侧肢体急性缺血(acute limb ischemia, ALI),这已成为V-A ECMO的一种重要并发症,并显著影响患者的预后[2]。近几年,肢体灌注保护策略(limb perfusion protection strategies, LPPS)被顺势提出,旨在改善V-A ECMO患者下肢远端灌注血流,进一步避免ALI的发生[3]。于同侧肢体留置下肢灌注管(distal perfusion catheter, DPC)是预防以及改善ALI的主要方式,当前,国内外绝大多数医院以及文献报道均采用经股浅动脉置管顺行性远端灌注的方法[4], 而经胫后动脉放置DPC以逆行性远端灌注的方式却鲜有提及,而这也是一种留置DPC的可行方法。本研究回顾性分析在V-A ECMO中经胫后动脉留置DPC以逆行性远端灌注的患者的临床资料,以期为留置逆行性DPC提供进一步的经验。
1 资料与方法 1.1 研究对象收集2022年1月至2023年6月期间于本院重症医学科完成的15例V-A ECMO并行逆行性远端灌注的成人患者的病例数据。相关患者均知情同意。本研究伦理审批号:YX200710。
1.2 置管方式 1.2.1 V-A ECMO置管V-A ECMO置管分为手术切开与经皮穿刺两种方式。本院经验,当血流动力学不稳定或处于心肺复苏时,此时因血管收缩等易导致穿刺困难,为保证一次性置管成功,选择手术切开,过程简略如下:于右侧或左侧腹股沟区(优先右侧)行横行切口约5 cm,逐层游离,至少彻底显露股动脉、股静脉前壁,以5-0 Prolene滑线于股动、静脉插管处预留荷包线,穿刺置入导丝后置管并收紧荷包线以防出血。当血流动力学尚稳定时,则选择在超声引导下或盲穿,按照Seldinger法经皮穿刺置管,过程简略如下:于右侧或左侧腹股沟区(优先右侧)行股动脉、股静脉穿刺,置入导丝,依次扩皮后置管。通常,不论手术切开还是经皮穿刺,股静脉选择放置21 F插管,深度40~45 cm,股动脉放置17 F插管,深度20 cm。
1.2.2 DPC置管V-A ECMO置管方式决定了DPC放置的方式。手术切开置管时,因是在直视下操作,且因血流动力学不稳定等因素导致血管变细,故皆会在装机同时于直视下行预防性股浅动脉顺行性DPC置管,过程简略如下:暴露股动脉后,在股动脉插管以远股浅动脉处,预置荷包线,并反向穿刺留置8 F或6 F鞘管,最后收紧荷包止血。经皮穿刺置管时,可选择在股浅动脉处按照Seldinger法经皮穿刺顺行性留置股动脉鞘管,但此时往往会因为血管变细以及操作空间狭窄等因素造成穿刺困难,常会导致反复多次穿刺而不成功情况发生,而此时亦可选择经胫后动脉留置DPC以逆行性远端灌注,过程如下:股动脉置管同侧腿外旋以暴露内侧踝关节,于内踝后方作一长4~5 cm横行切口,逐层分离皮下以及肌肉组织,胫后动脉位置表浅,逐层分离即可探查见胫后动脉以及两条伴行静脉,将位于中间的胫后动脉充分游离,因胫后动脉较细,此时也可用丝线将其悬吊以方便穿刺,最后按照Seldinger法经皮置入导丝,留置6 F或8 F鞘管并连接ECMO环路动脉侧分支(图 1A、图 1B、图 1C)。从DPC鞘管流出的血液会逆行流到腘动脉的三分岔处(腘动脉三个分支:胫前动脉、胫后动脉、腓动脉)并灌注到整个肢体[5]。
|
| A:探查到的胫后动脉;B:于胫后动脉置入8 F鞘管;C:8 F鞘管连接ECMO环路动脉侧分支行逆行性远端灌注 图 1 手术切开方式经胫后动脉置入DPC Fig 1 Inserting DPC through the posterior tibial artery by surgical incision |
|
|
本院所有V-A ECMO患者均于手术室内行V-A ECMO撤机术以及股动脉修补术、股静脉缝合术,过程简略如下:彻底显露股动脉、股静脉、顺行DPC插管处,股动脉插管处留置两圈荷包,其余留置一圈荷包,拔除各处插管后收紧荷包;如是经胫后动脉逆行性DPC,则可直接拔除鞘管并按压止血30 min。若胫后动脉损伤,必要时可行胫后动脉结扎术[6]。
1.4 下肢缺血判定ALI的判断主要基于5P症(苍白、无脉、感觉异常、肢体麻痹与疼痛)以及多普勒超声对下肢血运的动态监测。清醒患者主要基于主观感觉,当出现麻木、疼痛等感觉甚至逐渐加重时,则应考虑ALI的可能;无意识患者主要基于与对侧下肢的对比,当ECMO动脉插管侧肢体出现皮肤苍白、皮温凉、花斑等变化时则应考虑ALI的可能[7]。ALI的判定需及时识别并立即处理,以免出现骨筋膜室综合征、肢体末端坏死甚至截肢等严重并发症。
1.5 统计学方法应用SPSS 27.0统计学软件进行数据分析。计量资料以均数±标准差(x±s)表示,计数资料以例(%)表示。
2 结果 2.1 一般数据本研究共纳入15例V-A ECMO并行逆行性DPC的成人患者,均为经皮穿刺置管。清醒3例,镇静8例,昏迷4例;暴发性心肌炎5例,急性心肌梗死7例,扩张型心肌病、恶性心律失常、肺栓塞各1例;盲穿9例,超声引导穿刺6例;动脉插管型号为17F 13例,15F 2例;康复10例,包括心脏移植后康复1例,死亡5例。见表 1。
| 项目 | 例(%) | 项目 | 例(%) |
| 意识状态 | 疾病类型 | ||
| 清醒 | 3(20.00) | 暴发性心肌炎 | 5(33.33) |
| 镇静 | 8(53.33) | 急性心肌梗死 | 7(46.67) |
| 昏迷 | 4(26.67) | 扩张型心肌病 | 1(6.67) |
| 穿刺置管 | 恶性心律失常 | 1(6.67) | |
| 盲穿 | 9(60.00) | 肺栓塞 | 1(6.67) |
| 超声引导 | 6(40.00) | 预后 | |
| 插管型号 | 康复 | 10(66.67) | |
| 17F | 13(86.67) | 死亡 | 5(33.33) |
| 15F | 2(13.33) |
15例患者均为经胫后动脉留置DPC。V-A ECMO装机时,为预防下肢缺血发生,同时留置DPC则为预防性置管;V-A ECMO装机后,发现下肢缺血症状时再行DPC置管则为补救性置管。预防性置管6例,于V-A ECMO装机后2 h内完成,补救性置管9例,根据症状以及临床表现判定为下肢缺血后置入;一次性置管成功率较高,为93.33%;导管型号选择以6 F鞘管为主,占66.67%;所有预防性置管无ALI发生,补救性置管中发生1例骨筋膜室综合征;置管时间为(20.73±3.47)min。见表 2。
| 项目 | 数据 | 项目 | 数据 | |
| 灌注方式a | 导管型号a | |||
| 胫后动脉逆行性 | 15(100.00) | 5F | 1(6.67) | |
| 置管时机a | 6F | 10(66.67) | ||
| 预防性(< 2 h) | 6(40.00) | 8F | 4(26.67) | |
| 补救性 | 9(60.00) | 下肢预后a | ||
| 诉麻木 | 2(13.33) | 预防性 | 6(40.00) | |
| 诉疼痛 | 1(6.67) | 有ALI发生 | 0(0.00) | |
| 下肢花斑 | 5(33.33) | 无ALI发生 | 6(40.00) | |
| 下肢苍白、皮温凉 | 1(6.67) | 补救性 | 9(60.00) | |
| 一次置管成功a | 恢复正常 | 8(53.33) | ||
| 是 | 14(93.33) | 骨筋膜室综合征 | 1(6.67) | |
| 否 | 1(6.67) | 置管时间b | 20.73±3.47 | |
| DPC为下肢灌注管,a数据为[例(%)],b数据为(min, x±s) | ||||
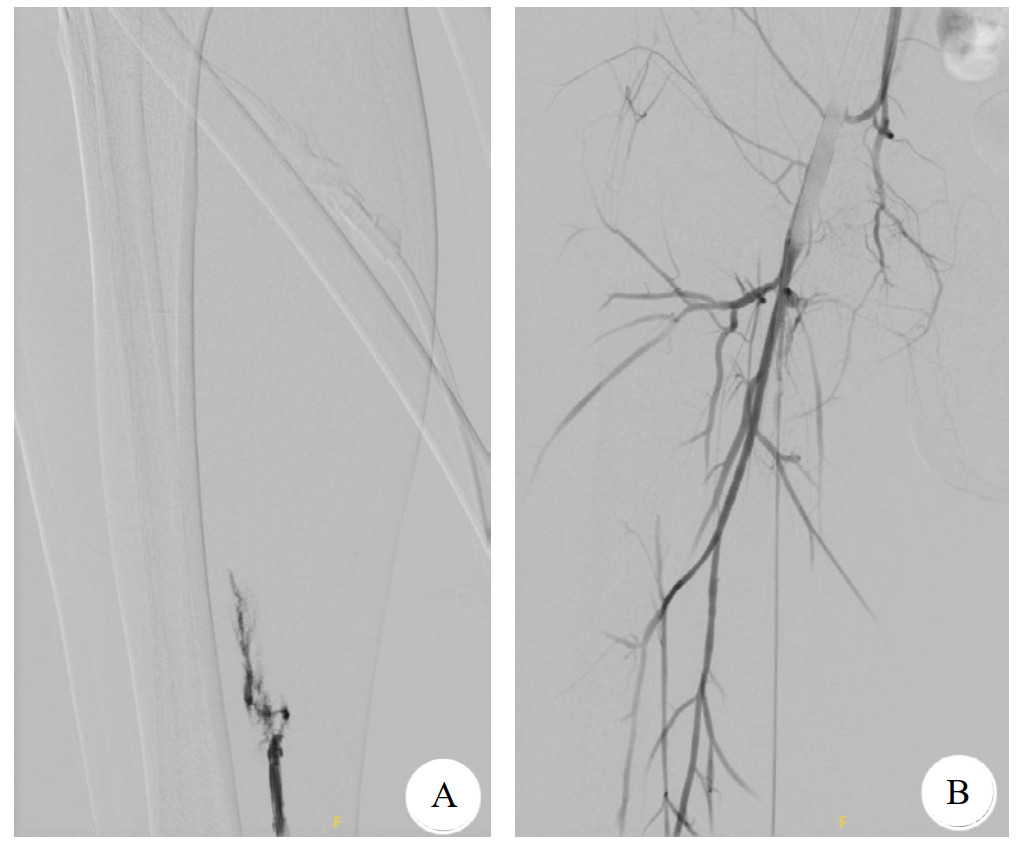
一次性置管失败发生1例,并在置管后逐渐发展为骨筋膜室综合征,立即行下肢动脉造影术以及小腿切开减张负压吸引术。在造影下经判定误穿胫后动脉夹层(图 2A),遂在术中横行切开胫后动脉前壁,在造影确认下进入血管真腔,置入5 F血管鞘,再次造影示股浅动脉、股深动脉、腘动脉、胫后动脉等动脉通畅(图 2B)后连接ECMO环路动脉侧分支。该次造影显示血液可经胫后动脉逆行至腘动脉三分岔处以及股深动脉分支处,进一步证实了经胫后动脉逆行性灌注是完全可行的。
|
| A:鞘管误入胫后动脉夹层,造影剂无法顺利上行;B:鞘管置入胫后动脉真腔,逆行造影可见股浅动脉、股深动脉、腘动脉、胫后动脉等显影 图 2 V-A ECMO置管侧下肢动脉造影 Fig 2 Lower limb arterial angiography on the side of V-A ECMO catheterization |
|
|
虽然V-A ECMO的动脉插管可选用股动脉、腋动脉以及颈总动脉等,但因股动脉位置表浅,更加便于操作,因而使得经股静脉、股动脉置管成为V-A ECMO建立的最常见路径,但与此同时所带来的下肢缺血并发症也已经成为不容忽视的问题,多项临床研究[8-10]证实,在V-A ECMO中ALI发生率高达10%~70%,截肢发生率亦为1.9%~4.7%。造成ALI的原因来自多方面,动脉插管可直接造成股动脉狭窄甚至闭塞,同时血流动力学的不稳定、血管活性药物的应用可导致血管直径缩小,此外,股动脉血管内皮的损伤、非搏动性血流、血栓的形成等都可导致插管侧下肢远端供血相对或绝对不足,从而造成下肢缺血。ALI的发生对于危重患者来说属于“二次打击”[10],相关文献[2, 4, 11-13]指出,下肢缺血并发症是降低V-A ECMO患者生存率的独立危险因素,显著影响患者的预后。
于同侧肢体留置DPC是目前公认的能明确改善下肢缺血的方法[4, 9, 14-15],尽管不能完全杜绝ALI的发生,但可以将ALI发生率降低至6.5%~8.6%[10, 16]。在同侧股浅动脉留置顺行性DPC是最常用的办法,可以于手术切开装机时放置,也可以在床旁彩超、血管造影[14]引导下操作。但顺行性DPC的置入并不容易,特别是在补救性置管的情况下,由于动脉插管侧远端血管塌陷,穿刺置管极易出现失败,常需反复多次穿刺,从而导致血肿、损伤血管或误穿股静脉等情况的出现,造成不良后果。
自2012年Spurlock等[6]首次报道了经胫后动脉留置逆行性DPC这一新技术以来,该方式并未得到全面应用,相关文献罕见。原因可能在于一是因为该技术为手术切开置管,需要外科医生来实施,技术上较顺行性DPC要稍复杂,其次是因为多数医疗人员可能对该技术并不了解或对其可行性存在疑惑。本院ECMO中心医师均为外科医师,可全面实施该技术,该技术要点:①胫后动脉位置表浅,通常位于内踝内后侧一厘米的地方。②胫后动脉一般具有两条伴行静脉,动脉则位于两条静脉之间。③探查到胫后动脉之后,以Seldinger法置入动脉鞘管,穿刺时一定回抽见血,确保进入血管真腔内。在DPC鞘管型号选择方面,王露平等[17]以53例V-A ECMO患者为研究对象研究后认为以6 F鞘管最为合适,同时,郭剑等[18]报道选用8 F鞘管可造成11.76%的下肢过度灌注,Laimoud等[19]则提出在满足远端灌注的前提下,最好选用较小型号的DPC插管,以避免动脉内膜损伤、血栓形成、插管困难等情况的发生。本次研究选用5 F、6 F、8 F鞘管均满足了灌注需要且未造成奢灌,且下肢动脉造影显示以5 F型号鞘管亦可逆行提供足够的血流,其次,Spurlock等[6]认为逆行性远端灌注管平均流量需维持在155.8 mL/min方可满足灌注需要,因此或许只要控制灌注流量在一定水平时,可根据实际胫后动脉血管情况选取不同型号的鞘管。
关于DPC置入时机,尽管不同文献报道不一,但积极放置要优于消极等待这一理念已得到更多人的认可[20]。此外,DPC的置入并非一劳永逸,仍存在ALI的可能,同时置入DPC造成的血肿、血栓形成、血管损伤等都可能加重下肢缺血的严重程度,临床中仍需密切关注下肢血运变化[21]。
综上所述,在V-A ECMO中,经胫后动脉放置DPC以逆行性远端灌注的方式是完全可行的,可预防或治疗下肢缺血。本研究为回顾性临床研究,样本量有限,存在一定的局限性,仍需进一步扩大样本量以深入研究。
利益冲突 所有作者声明无利益冲突
作者贡献申明 李坤,丁丹丹:实验操作、论文撰写;马瑞科,韩佃明,高宗炜,杜沂峰:数据收集及整理、统计学分析;尚庆娟:研究设计、论文修改
| [1] | Lorusso R, Shekar K, MacLaren G, et al. ELSO interim guidelines for venoarterial extracorporeal membrane oxygenation in adult cardiac patients[J]. ASAIO J, 2021, 67(8): 827-844. DOI:10.1097/MAT.0000000000001510 |
| [2] | Hu SX, Lu AD, Pan CL, et al. Limb ischemia complications of veno-arterial extracorporeal membrane oxygenation[J]. Front Med, 2022, 9: 938634. DOI:10.3389/fmed.2022.938634 |
| [3] | Marbach JA, Faugno AJ, Pacifici S, et al. Strategies to reduce limb ischemia in peripheral venoarterial extracorporeal membrane oxygenation: a systematic review and Meta-analysis[J]. Int J Cardiol, 2022, 361: 77-84. DOI:10.1016/j.ijcard.2022.04.084 |
| [4] | Blakeslee-Carter J, Shao C, LaGrone R, et al. Vascular complications based on mode of extracorporeal membrane oxygenation[J]. J Vasc Surg, 2022, 75(6): 2037-2046.e2. DOI:10.1016/j.jvs.2022.01.078 |
| [5] | Babu A. Techniques for venoarterial extracorporeal membrane oxygenation support and conversion to temporary left ventricular assist device[J]. Oper Tech Thorac Cardiovasc Surg, 2014, 19(3): 365-379. DOI:10.1053/j.optechstcvs.2014.11.003 |
| [6] | Spurlock DJ, Toomasian JM, Romano MA, et al. A simple technique to prevent limb ischemia during veno-arterial ECMO using the femoral artery: the posterior tibial approach[J]. Perfusion, 2012, 27(2): 141-145. DOI:10.1177/0267659111430760 |
| [7] | Björck M, Earnshaw JJ, Acosta S, et al. Editor's choice - European society for vascular surgery (ESVS) 2020 clinical practice guidelines on the management of acute limb ischaemia[J]. Eur J Vasc Endovasc Surg, 2020, 59(2): 173-218. DOI:10.1016/j.ejvs.2019.09.006 |
| [8] | Yang F, Hou DB, Wang JH, et al. Vascular complications in adult postcardiotomy cardiogenic shock patients receiving venoarterial extracorporeal membrane oxygenation[J]. Ann Intensive Care, 2018, 8(1): 72. DOI:10.1186/s13613-018-0417-3 |
| [9] | Yau P, Xia Y, Shariff S, et al. Factors associated with ipsilateral limb ischemia in patients undergoing femoral cannulation extracorporeal membrane oxygenation[J]. Ann Vasc Surg, 2019, 54: 60-65. DOI:10.1016/j.avsg.2018.08.073 |
| [10] | 张晓玲, 陈琨, 徐晓, 等. 基于下肢灌注评估表置入远端灌注导管与预防性置入远端灌注导管在ECMO中的疗效比较[J]. 中华危重病急救医学, 2021(12): 1484-1490. |
| [11] | Minc SD, Hayanga HK, Thibault D, et al. Vascular complications increase hospital charges and mortality in adult patients on extracorporeal membrane oxygenation in the United States[J]. Semin Thorac Cardiovasc Surg, 2021, 33(2): 397-406. DOI:10.1053/j.semtcvs.2020.09.025 |
| [12] | Pahuja M, Ranka S, Chehab O, et al. Incidence and clinical outcomes of bleeding complications and acute limb ischemia in STEMI and cardiogenic shock[J]. Catheter Cardiovasc Interv, 2021, 97(6): 1129-1138. DOI:10.1002/ccd.29003 |
| [13] | 孟庆冰, 沙宣伊, 高恒波, 等. 自制改良远端灌注延长管在股静动脉体外膜肺氧合中的应用[J]. 中华急诊医学杂志, 2022, 31(11): 1553-1554. DOI:10.3760/cma.j.issn.1671-0282.2022.11.026 |
| [14] | Shah A, Arons D, Pasrija C, et al. Bedside angiography of distal perfusion catheter for veno-arterial extracorporeal membrane oxygenation[J]. Perfusion, 2022, 37(5): 499-504. DOI:10.1177/02676591211007017 |
| [15] | Kaufeld T, Beckmann E, Ius F, et al. Risk factors for critical limb ischemia in patients undergoing femoral cannulation for venoarterial extracorporeal membrane oxygenation: Is distal limb perfusion a mandatory approach?[J]. Perfusion, 2019, 34(6): 453-459. DOI:10.1177/0267659119827231 |
| [16] | Kaushal M, Schwartz J, Gupta N, et al. Patient demographics and extracorporeal membranous oxygenation (ECMO)-related complications associated with survival to discharge or 30-day survival in adult patients receiving venoarterial (VA) and venovenous (VV) ECMO in a quaternary care urban center[J]. J Cardiothorac Vasc Anesth, 2019, 33(4): 910-917. DOI:10.1053/j.jvca.2018.08.193 |
| [17] | 王露平, 韩小彤, 李想, 等. 同时置入6F血管鞘用于远端灌注在股动静脉体外膜肺氧合中安全性及有效性的评估[J]. 中国急救医学, 2021, 41(7): 624-629. DOI:10.3969/j.issn.1002-1949.2021.07.020 |
| [18] | 郭剑, 卢安东, 苗莉霞, 等. 经股动静脉体外膜肺氧合下肢并发症的防治及管理策略[J]. 中国体外循环杂志, 2019, 17(1): 22-25. DOI:10.13498/j.cnki.chin.j.ecc.2019.01.06 |
| [19] | Laimoud M, Saad E, Koussayer S. Acute vascular complications of femoral veno-arterial ECMO: a single-centre retrospective study[J]. 2021, 73(1): 15. DOI: 10.5194/bg-10-1219-2013. |
| [20] | Black MC, Slaughter MS. Proactive or reactive? Best approach to limb ischemia in peripheral venoarterial extracorporeal life support[J]. J Thorac Cardiovasc Surg, 2016, 151(6): 1745-1746. DOI:10.1016/j.jtcvs.2015.11.064 |
| [21] | 周利平, 黄国庆, 李湘民, 等. 体外膜肺氧合治疗期间出血和血栓事件的危险因素分析[J]. 中华急诊医学杂志, 2023, 32(9): 1226-1234. DOI:10.3760/cma.j.issn.1671-0282.2023.09.014 |
 2024, Vol. 33
2024, Vol. 33