2. 阜外华中心血管病医院营养科,郑州 451464;
3. 阜外华中心血管病医院冠心病重症监护室,郑州 451464;
4. 阜外华中心血管病医院体外循环科,郑州 451464
2. Department of Nutrition, FuWai Central China Cardiovascular Hospital, Zhengzhou 451464, China;
3. Coronary Heart Disease Intensive Care Unit, FuWai Central China Cardiovascular Hospital, Zhengzhou 451464, China;
4. Department of Extracorporeal Circulation, FuWai Central China Cardiovascular Hospital, Zhengzhou 451464, China
体外膜肺氧合(extracorporeal membrane oxygenation, ECMO)是一项为危重呼吸/心脏衰竭患者提供呼吸或循环支持的机械技术,其中静脉-动脉体外膜肺氧合(veno-arterial extracorporeal membrane oxygenation, VA-ECMO)主要用于心脏衰竭患者[1]。需要ECMO支持的患者往往起病急,病情重,属于重症患者中更为危重的人群;此类患者机体处于分解代谢增加,胰岛素抵抗,负氮平衡的状态,能量和蛋白质需求增加,因此营养支持对于纠正营养不良,降低并发症发生率,促进康复起关键作用[2-3]。在ECMO患者中早期肠内营养支持(early enteral nutrition, EEN)是安全和可耐受的,但达到营养目标仍具有挑战性[4];其平均营养支持达标率偏低,VA-ECMO的平均达标率仅为50%。而喂养不达标可能与重症患者住院时间延长、感染等并发症的发生以及住院病死率升高有关[5-6]。
河南省人民医院自2021年成立由冠心病重症监护室(coronary heart disease intensive care unit, CCU)、心脏外科、体外循环科、神经内科、呼吸内科、肾内科、消化内科、药学部、临床营养科等组成的ECMO多学科团队,其中营养师参与讨论并制定ECMO患者个体化营养支持目标和方案。目前仍缺乏关于成人ECMO患者最佳营养管理的数据,故本研究回顾性分析本院VA-ECMO患者早期EN达标对其预后的影响,旨在为ECMO患者的临床营养治疗方案提供循证依据,现报道如下。
1 资料与方法 1.1 研究对象回顾性收集2022年2月至2023年3月就诊于河南省人民医院CCU的VA-ECMO成人患者资料。纳入标准:(1)年龄≥18岁;(2)住院时间≥7 d;(3)ECMO开始后48 h内给予EN支持;(4)临床病历资料记录完整清晰。排除标准:(1)终末期多器官功能衰竭患者;(2)ECMO期间未行EN支持;(3)因经济原因等自动离院。共61例患者纳入研究,其中男性44例,女性17例,年龄(58.46±13.71)岁。根据重症营养指南建议[7],对于采用预测公式计算目标能量的重症患者,应在第一周内使用低热卡营养支持治疗(低于目标能量的70%),故以ECMO开始后第7天时EN摄入量是否达到目标能量的70%,将患者分为达标组(34例)和未达标组(27例)。本研究符合医学伦理学标准,伦理审批号为(2023)伦审第(156)。
1.2 营养支持所有患者入住CCU后的营养风险筛查(NRS2002)评分均≥3分,存在营养风险,需要进行营养支持。(1)启动时机:循环稳定的患者,排除EN禁忌证(如消化道出血、肠梗阻等)后于ECMO开始后24~48 h内尽早启动EN。(2)目标能量:欧洲临床营养与代谢学会(ESPEN)推荐在应激早期每日能量为20~25 kcal/kg,对于稳定的患者可增加至25~30 kcal/kg。本研究暂以25 kcal/kg计算目标能量,对于体型正常和消瘦的患者,采用实际体重;对于肥胖患者,采用校正体重,即理想体重+0.4×超重体重。(3)方案:根据患者胃肠耐受情况选择百普力(短肽型)或能全力(1.0/1.5,整蛋白型),初始泵速为20 mL/h,循序渐进增加泵速至目标能量。(4)监测:营养护士定期评估患者EN耐受情况和营养制剂的吸收状况(如肠鸣音和胃潴留量等)。营养师和临床医师联合查房,酌情调整营养方案,必要时使用胃肠动力或止泻药物、幽门后喂养等。如无效则加用肠外营养。
1.3 数据收集根据病历和护理系统采集患者的身高、体重、性别、年龄、入院诊断、入院时的营养风险指数(nutritional risk index, NRI)、急性生理与慢性健康状况(acute physiology and chronic health evaluation Ⅱ, APACHE Ⅱ)评分、ECMO支持的原因、ECMO模式、ECMO持续时间、ECMO支持前3 d的平均乳酸值、出入平衡量、射血分数及相关血液指标(白蛋白、血红蛋白、淋巴细胞计数)、CCU停留时间、住院时间、住院费用、机械通气、ECMO期间消化道出血、细菌感染、缺血缺氧性脑病发生情况以及是否联合持续肾脏替代治疗(continuous renal replacement therapy, CRRT)、是否采用主动脉球囊反搏(intra-aortic balloon pump, IABP)辅助循环、出院存活情况等信息。计算患者的目标能量和ECMO开始7 d内EN摄入量及其占目标能量的比值。
1.4 统计学方法采用SPSS 23.0软件进行统计分析。计量资料符合正态分布,以均数±标准差(x±s)表示;不符合正态分布则以中位数(四分位数)[M(Q1, Q3)]表示。两组比较采用独立样本t检验或秩和检验。计数资料以频数和百分比表示,组间比较采用χ2检验。不同组别患者生存时间的比较采用Kaplan-Meier法Log-Rank检验。采用单因素和多因素Cox比例风险模型分析相关因素对住院病死率的影响。采用受试者特征曲线(receiver operator characteristic curve, ROC)法分析ECMO开始7 d内EN摄入量占目标能量的比值对患者预后情况的筛检率、切点值,分别用ROC曲线下面积(area under the curve, AUC)、敏感度、特异度表示。以P < 0.05为差异有统计学意义。
2 结果 2.1 基线情况达标组和未达标组在年龄、性别、BMI、APACHE Ⅱ评分、NRI、适用ECMO的原因分布、ECMO持续时间、启动EN时间、ECMO期间使用IABP、血管药物使用≥3种、ECMO开始前3 d的平均乳酸值和出入平衡量、ECMO开始时血液指标如血红蛋白和白蛋白水平、淋巴细胞计数等方面均差异无统计学意义(均P > 0.05)。两组患者一般资料均衡,具有可比性。见表 1。
| 项目 | 达标组(n=34) | 未达标组(n=27) | t/χ2/Z | P值 |
| 年龄(岁)a | 56.32±12.32 | 61.15±15.08 | -1.375 | 0.174 |
| 男(n, %) | 21(61.76) | 23(85.18) | 4.106 | 0.050 |
| BMI(kg/m2)a | 23.76±2.99 | 25.19±3.64 | -1.687 | 0.097 |
| APACHE Ⅱ评分(分)a | 24.41±3.77 | 26.11±3.54 | -1.794 | 0.078 |
| NRI a | 94.36±6.95 | 93.78±6.99 | 0.330 | 0.743 |
| 适用ECMO的原因(n, %) | 6.814 | 0.078 | ||
| 心肌梗死 | 15(44.11) | 9(33.33) | ||
| 心脏骤停 | 3(8.82) | 9(33.33) | ||
| 爆发性心肌炎 | 7(20.59) | 2(7.41) | ||
| 其他, 如术后心衰等 | 9(26.48) | 7(25.93) | ||
| ECMO持续时间(d)a | 8.38±3.38 | 8.18±3.49 | 0.223 | 0.825 |
| ECMO支持后启动EN时间(h)a | 7.29±5.50 | 10.42±8.50 | -1.283 | 0.204 |
| ECMO期间使用IABP(n, %) | 26(76.47) | 19(70.37) | 0.289 | 0.770 |
| ECMO期间血管药物使用≥3种(n, %) | 8(23.53) | 12(44.44) | 2.987 | 0.084 |
| ECMO开始前3 d平均乳酸值(mmol/L)a | 3.71±2.87 | 5.12±3.56 | -1.720 | 0.091 |
| ECMO开始前3 d平均出入平衡量(mL)b | -564.61(-835.62, 112.38) | -230.06(566.73, 253.4) | -1.583 | 0.113 |
| ECMO开始时的射血分数(%)a | 38.21±13.81 | 36.52±10.44 | 0.526 | 0.601 |
| ECMO开始时的血液指标 | ||||
| Pro-BNP(pg/mL)b | 3153.50(1317.50, 5140.25) | 1980.00(607.00, 5498.00) | -0.850 | 0.396 |
| 白蛋白(g/L)a | 36.18±5.73 | 34.67±5.27 | -1.062 | 0.292 |
| 血红蛋白(g/L)a | 124.18±25.15 | 119.48±23.72 | 0.742 | 0.461 |
| 淋巴细胞计数(×109/L)a | 1.24±0.76 | 1.24±0.89 | -0.010 | 0.992 |
| 注:a为(x±s),b为M(Q1, Q3;BMI为体脂指数,APACHE Ⅱ为急性生理与慢性健康状况评分,NRI为营养风险指数,ECMO为体外膜肺氧合,EN为肠内营养,IABP为主动脉球囊反驳,Pro-BNP为B型利钠肽原 | ||||
达标组和未达标组在ECMO期间细菌感染、消化道出血、缺血缺氧性脑病的发生情况以及CCU停留时间、住院时间、住院费用等方面差异无统计学意义(均P > 0.05)。而未达标组患者ECMO期间机械通气率和住院病死率均高于达标组,差异有统计学意义(均P < 0.05)。见表 2。
| 项目 | 达标组(n=34) | 未达标组(n=27) | t/χ2 | P值 |
| ECMO期间并发细菌感染(n, %) | 20(58.82) | 19(70.37) | 0.870 | 0.351 |
| ECMO期间并发消化道出血(n, %) | 14(41.18) | 12(44.44) | 0.066 | 1.000 |
| ECMO期间缺血缺氧脑病(n, %) | 11(32.35) | 14(51.85) | 2.366 | 0.124 |
| ECMO期间CRRT(n, %) | 13(38.24) | 14(51.85) | 1.131 | 0.312 |
| ECMO期间进行机械通气(n, %) | 22(64.71) | 24(88.88) | 4.746 | 0.038 |
| CCU停留时间(d)a | 16.44±6.75 | 14.93±6.08 | 0.909 | 0.367 |
| 住院时间(d)a | 21.50±10.29 | 19.55±11.78 | 0.687 | 0.495 |
| 住院总费用(万元)a | 40.65±3.08 | 37.11±2.77 | 0.834 | 0.408 |
| 出院时死亡(n, %) | 11(32.35) | 19(70.37) | 8.703 | 0.003 |
| 注:ECMO为体外膜肺氧合,CRRT为持续肾脏替代治疗,CCU为冠心病重症监护室;a为(x±s) | ||||
| 参数 | 单因素分析 | 多因素分析 | |||||
| β值 | HR (95%CI) | P值 | β值 | HR (95%CI) | P值 | ||
| 年龄 | 0.447 | 1.564 (0.759~3.222) | 0.225 | ||||
| 性别(男性) | 0.880 | 2.410 (0.912~6.367) | 0.076 | ||||
| ECMO期间并发细菌感染 | 1.000 | 2.719 (1.040~7.108) | 0.041 | ||||
| ECMO期间并发消化道出血 | 0.878 | 2.406 (1.153~5.017) | 0.019 | ||||
| ECMO期间缺血缺氧性脑病 | 1.165 | 3.205 (1.534~6.700) | 0.002 | 1.076 | 0.341 (0.119~0.975) | 0.045 | |
| ECMO期间CRRT | 0.810 | 2.248 (1.068~4.731) | 0.033 | ||||
| ECMO期间使用IABP | -0.231 | 0.793 (0.323~1.947) | 0.613 | ||||
| ECMO开始前3 d乳酸升高 | 0.292 | 1.339 (0.630~2.847) | 0.447 | ||||
| ECMO期间撤机失败 | 1.649 | 5.204 (2.414~11.216) | < 0.001 | 1.312 | 0.269 (0.111~0.651) | 0.004 | |
| ECMO第7天EN达标 | -3.303 | 0.037 (0.005~0.271) | 0.001 | -2.388 | 10.891 (1.178~100.718) | 0.035 | |
| 注:ECMO为体外膜肺氧合,CRRT为持续肾脏替代治疗,IABP为主动脉球囊反驳 | |||||||
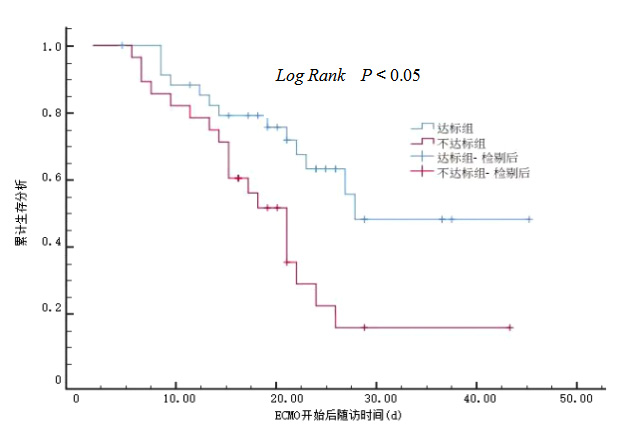
生存分析结果显示,达标组患者住院生存率(67.65%)高于未达标组(29.63%),两组比较差异有统计学意义(P < 0.05)(图 1)。
|
| 图 1 两组患者住院生存曲线分析 Fig 1 Analysis of hospitalization survival curves for two groups of patients |
|
|
通过COX比例风险模型对可能导致ECMO患者住院死亡的多种因素进行单因素分析,结果显示患者ECMO期间有严重并发症,如细菌感染、消化道出血、缺血缺氧性脑病以及、CRRT治疗及撤机失败与患者住院死亡呈正相关关系;而ECMO第7天EN达标与患者住院死亡呈负相关关系,差异均具有统计学意义(均P < 0.05)。多因素分析结果显示,ECMO辅助期间并发缺血缺氧性脑病、撤机失败及ECMO第7天EN达标与患者住院死亡相关(HR=0.341,95%CI: 0.119~0.975,P < 0.05;HR=0.269,95%CI: 0.111~0.651,P < 0.05;HR=10.891,95%CI: 1.178~100.718,P < 0.05)。
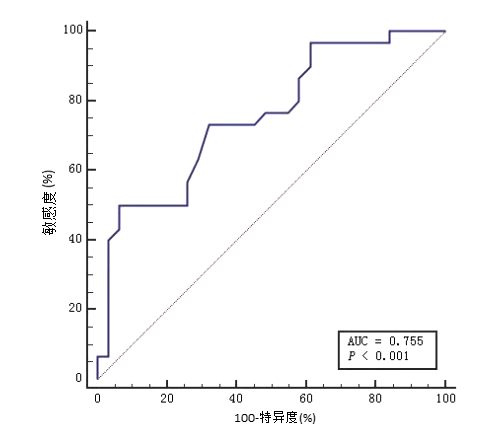
2.4 EN占目标能量的比值预测患者住院死亡的ROC曲线分析绘制ECMO开始7 d内EN摄入量占目标能量比值预测患者住院死亡的ROC曲线。结果显示:ECMO第7天EN占目标能量比值的AUC最高(0.755),特异度和敏感度分别为93.60%和50.00%,Youden指数为0.435,截断值(cut-off)为0.73(图 2)。
|
| 图 2 ECMO第7天EN摄入量占目标能量比值预测出院死亡ROC曲线 Fig 2 Predicting discharge mortality ROC curve using the ratio of EN intake to target energy on the 7th day of ECMO |
|
|
VA-ECMO作为难治性心源性休克患者的挽救性治疗手段,随着适应证的增加,目前临床应用越来越广泛[7-8]。但在VA-ECMO治疗过程中,患者往往处于严重的炎症和应激状态,机体极易出现代谢紊乱和肌肉消耗。同时由于血流动力学不稳定会影响肠道吸收和代谢,造成免疫抑制和肠道粘膜损伤,影响营养物质的吸收[9]。合理的营养供应不仅能满足其能量需求,维持正常的心肌收缩功能,还能帮助改善心脏功能,减少心肌储备的损耗,此外对于降低感染等并发症发生,改善患者的临床结局等都有重要意义[10]。因此探究VA-ECMO患者的营养支持特点,并分析营养支持与预后之间的关系,对于针对性改善营养治疗措施有重要意义。
本研究61例接受VA-ECMO治疗患者存活率为50.82%,高于卢桂阳等[11]的研究结果(34.8%),可能是由于其观察是28 d的生存情况,而本研究是以出院时是否存活为观察指标,两者观察时间不一致。生存分析结果显示,ECMO辅助期间并发缺血缺氧性脑病、撤机失败及ECMO第7天EN达标是患者住院期间死亡的影响因素。高国栋等[12]对10年间142例接受ECMO治疗的患者回顾性分析发现,ECMO建立24 h的高乳酸水平、高血糖水平、胃肠道出血和合并多器官脏器衰竭综合征为患者院内死亡的危险因素。本研究也发现ECMO期间并发消化道出血、缺血缺氧性脑病者死亡风险较高,但回归结果仅显示合并缺血缺氧性脑病是其住院期间死亡发生的影响因素。这种结果可能与样本量和调查指标的时间不一致有关。既往研究显示,接受VA-ECMO患者院内感染率达35.2%,其中以呼吸道感染最多,且治疗期间细菌感染会大大增加死亡风险,影响患者的预后[13]。患者血流动力学不稳定及高负荷的血管升压药等会导致肠道功能受损,增加消化道出血的风险,进而导致EN难以早期实施,早期EN已被证实是降低VA-ECMO治疗后病死率的独立影响因素[14]。因此,应在VA-ECMO患者住院期间严格无菌操作,降低感染风险;评估胃肠功能后尽早启动EN,以有效提高患者治愈率。
为进一步明确早期EN对VA-ECMO住院患者的预测作用,采用ROC曲线明确其相关关系后发现,接受VA-ECMO后患者上机第7天的EN摄入量占目标能量的比值对患者出院前的病死率有重要预测价值,AUC曲线下面积为0.755,截断值为0.73。其结果表明接受VA-ECMO患者在治疗后第7天EN摄入量占目标能量比值在73%以上者,其院内生存率更高。Park等[10]也发现在VA-ECMO开始后的第8天达到其能量需求的70%,且当每日平均能量摄入量在8~14 d内增加目标的10%时,90 d病死率降低18%。早期EN对于ECMO患者是安全可行的,而达到营养目标仍具有挑战性,可能与诊断或治疗过程中的禁食、胃潴留等因素有关;但也有研究报告,60%的患者在ECMO的14 d内获得了 > 80%的能量目标[4]。王烁等[15]的综述阐述了危重病患者各期营养状态及营养治疗,其中建议急性晚期(ICU 3~7 d)患者的能量目标应为70%的预估值或80%~100%的测量值。这些结果均提示,在VA-ECMO危重症患者的治疗过程中,应加强对早期能量摄入量的关注。
综上所述,VA-ECMO患者的营养支持对于改善结局至关重要。通过合理的能量和蛋白质摄入,维持正氮平衡,减少炎症反应,改善心肌功能,并预防并发症的发生,可以提高患者的治疗效果和康复水平,最终改善结局。因此,在VA-ECMO治疗中,应该将营养支持纳入综合治疗策略的重要组成部分,确保患者获得合理的营养支持。本研究不足之处在于一方面回顾性研究可能存在一定的偏倚,但本研究采用了双人核对的方式尽量减少误差的发生;其次本研究样本量和观察指标较少,后续需要大规模前瞻性研究来验证本次研究结果。
利益冲突 所有作者声明无利益冲突
作者贡献声明 杨阳:酝酿和设计实验,实施研究,采集数据,分析/解释数据,起草文章,统计分析;许桢:酝酿和设计实验,实施研究,采集数据;孙经:酝酿和设计实验,实施研究,采集数据;杨婷婷:酝酿和设计实验,实施研究,采集数据,分析/解释数据,统计分析;焦翠:实施研究,采集数据;张晶晶:实施研究,采集数据;胡振杰:实施研究,采集数据,支持性贡献;李建朝:酝酿和设计实验,实施研究,采集数据,分析/解释数据,对文章的知识性内容作批评性审阅,统计分析,获取研究经费,行政、技术或材料支持,指导,支持性贡献
| [1] | Keebler ME, Haddad EV, Choi CW, et al. Venoarterial extracorporeal membrane oxygenation in cardiogenic shock[J]. JACC Heart Fail, 2018, 6(6): 503-516. DOI:10.1016/j.jchf.2017.11.017 |
| [2] | 张黎, 孙兵, 贺航咏, 等. 成人体外膜肺氧合患者的营养支持[J]. 中华临床营养杂志, 2016, 24(1): 53-57. DOI:10.3760/cma.j.issn.1674-635X.2016.01.011 |
| [3] | 王瑜, 时皎皎, 常硕, 等. 成人体外膜肺氧合支持病人的营养支持治疗研究进展[J]. 肠外与肠内营养, 2022, 29(5): 304-309. DOI:10.16151/j.1007-810x.2022.05.009 |
| [4] | Karpasiti T. A narrative review of nutrition therapy in patients receiving extracorporeal membrane oxygenation[J]. ASAIO J, 2022, 68(6): 763-771. DOI:10.1097/mat.0000000000001540 |
| [5] | Compher C, Bingham AL, McCall M, et al. Guidelines for the provision of nutrition support therapy in the adult critically ill patient: the American Society for Parenteral and Enteral Nutrition[J]. JPEN J Parenter Enteral Nutr, 2022, 46(1): 12-41. DOI:10.1002/jpen.2267 |
| [6] | Jaksic T, Hull MA, Modi BP, et al. A.S.P.E.N. Clinical guidelines: nutrition support of neonates supported with extracorporeal membrane oxygenation[J]. JPEN J Parenter Enteral Nutr, 2010, 34(3): 247-253. DOI:10.1177/0148607110369225 |
| [7] | Ling RR, Ramanathan K, Poon WH, et al. Venoarterial extracorporeal membrane oxygenation as mechanical circulatory support in adult septic shock: a systematic review and meta-analysis with individual participant data meta-regression analysis[J]. Crit Care, 2021, 25(1): 246. DOI:10.1186/s13054-021-03668-5 |
| [8] | Pineton de Chambrun M, Bréchot N, Combes A. Venoarterial extracorporeal membrane oxygenation in cardiogenic shock: indications, mode of operation, and current evidence[J]. Curr Opin Crit Care, 2019, 25(4): 397-402. DOI:10.1097/MCC.0000000000000627 |
| [9] | Bréchot N, Hajage D, Kimmoun A, et al. Venoarterial extracorporeal membrane oxygenation to rescue sepsis-induced cardiogenic shock: a retrospective, multicentre, international cohort study[J]. Lancet, 2020, 396(10250): 545-552. DOI:10.1016/S0140-6736(20)30733-9 |
| [10] | Park J, Heo E, Song IA, et al. Nutritional support and clinical outcomes in critically ill patients supported with veno-arterial extracorporeal membrane oxygenation[J]. Clin Nutr, 2020, 39(8): 2617-2623. DOI:10.1016/j.clnu.2019.11.036 |
| [11] | 卢桂阳, 徐颢, 宁耀贵, 等. 综合ICU中成人体外膜肺氧合并发症及对预后的危险因素分析[J]. 中国中西医结合急救杂志, 2021, 28(6): 697-701. DOI:10.3969/j.issn.1008-9691.2021.06.012 |
| [12] | 高国栋, 吕琳, 胡强, 等. 阜外医院10年间成人体外膜肺氧合支持治疗回顾: 治疗策略及影响因素分析[J]. 中华危重病急救医学, 2015, 27(12): 959-964. DOI:10.3760/cma.j.issn.2095-4352.2015.12.004 |
| [13] | 王红, 侯晓彤, 李呈龙, 等. 心脏术后体外膜肺氧合辅助患者的医院感染[J]. 中华胸心血管外科杂志, 2016, 32(7): 399-402. DOI:10.3760/cma.j.issn.1001-4497.2016.07.005 |
| [14] | Ohbe H, Jo T, Yamana H, et al. Early enteral nutrition for cardiogenic or obstructive shock requiring venoarterial extracorporeal membrane oxygenation: a nationwide inpatient database study[J]. Intensive Care Med, 2018, 44(8): 1258-1265. DOI:10.1007/s00134-018-5319-1 |
| [15] | 王烁, 郭树彬, 何新华. 急危重症患者与营养治疗[J]. 中华急诊医学杂志, 2020, 29(10): 1265-1272. DOI:10.3760/cma.j.issn.1671-0282.2020.10.001 |
 2024, Vol. 33
2024, Vol. 33