2. 中山大学附属第八医院急诊医学科,深圳 518033
急性中毒是指人体在短时间内暴露于高剂量的毒性物质之中,从而引发的一种代谢紊乱和器官功能障碍的病理状态。基于某三甲医院收治病例的流行病学调查显示,2019年前急性中毒发病率呈现持续上升态势,虽近两年病例数量呈现下降趋势[1],但该疾病对社会医疗资源造成的压力仍不容忽视。一项研究数据显示,急性中毒的发病率约为0.178%[2]。根据相关统计数据显示,急性中毒已位列我国全因死亡顺位第5位,其病死率占比达10.7%[3],这一流行病学特征充分印证了该病症的致命风险。在急性中毒临床救治体系中,呼吸循环系统功能的维持构成核心治疗环节。体外膜肺氧合(extracorporeal membrane oxygenation, ECMO)技术通过体外循环系统将静脉血导出,经人工膜肺氧合后回输体内,从而实现对衰竭心肺功能的代偿性支持[4]。针对常规治疗手段(包括机械通气和药物干预)难以维持生命体征的急性中毒诱发性呼吸循环衰竭病例,ECMO常常作为一种二线治疗手段,并且其作为一种高级生命支持技术已被证实具有显著的救治价值[5-6]。以急性一氧化碳中毒为例证分析,血红蛋白与一氧化碳的高亲和力结合可导致全身性氧输送障碍,进而引发多器官缺氧性损伤。此时,及时实施ECMO治疗,能够迅速改善患者的氧合状态,减轻缺氧对各器官的损害,显著提高患者的生存率[7-8]。相较于传统机械通气与血液净化,ECMO在心肺功能双重衰竭的极端情境下展现出不可替代的优势。其核心价值在于能够绕过受损的心肺器官,直接提供气体交换与循环支持,为毒物代谢与器官功能恢复争取关键的“时间窗”[9],这是常规支持手段难以实现的。
2 ECMO在急性中毒领域应用的历史回顾ECMO在急性中毒救治中的应用并非一蹴而就,其发展轨迹与体外生命支持技术的整体演进、临床经验的积累以及对中毒病理生理学认识的深化紧密相连。我们将其发展历程划分为以下三个关键阶段,其演变历程及关键里程碑事件见表 1。
| 时期 | 阶段特征 | 核心技术特点 | 主要挑战与局限 |
| 1970s-1980s | 动物实验与初步探索期 | 硅胶膜,滚压泵 | 技术不成熟,并发症发生率高;仅限于理论验证和极少数个案尝试 |
| 1990s-2000s | 临床认知深化与适应证拓展期 | 中空纤维氧合器(聚丙烯)逐渐应用,设备有所改进 | 缺乏标准化的抗凝和管理方案;病例多为散在报道,证据等级低;对适用人群选择经验不足 |
| 2010s-至今 | 技术集成与系统化应用期 | PMP膜氧合器成为主流,离心泵普及,设备小型化、智能化 | 如何精准把握上机时机和撤离指征;不同毒物中毒患者制定个体化抗凝与管理策略;成本-效益比的优化 |
| 注:ECMO为体外膜肺氧合,PMP为聚甲基戊烯 | |||
初期研究主要基于动物实验模型,通过构建急性中毒动物模型体系,系统评估ECMO干预对中毒症状改善及生存率的影响[10]。实验数据显示,尽管ECMO技术可暂时性维持实验动物的基础生命体征,但由于受限于当时的技术成熟度不足及中毒病理机制认知缺陷,整体治疗效能未能实现显著性提升。1982年,Freedman等[11]进行了一项具有重要意义的实验,通过静脉注射利多卡因诱导犬心搏骤停,然后分别给予ECMO或标准复苏治疗。研究发现接受ECMO支持的犬全部存活,而接受标准复苏治疗的犬死亡率高达75%。这一实验成功证实了ECMO在致命性利多卡因中毒中替代心肺功能、维持生命直至毒物代谢清除的核心价值,为后续临床转化提供了坚实的实验依据。然而,受限于当时的设备性能(如硅胶膜氧合器易致血浆渗漏、凝血功能障碍)和临床管理经验匮乏,ECMO的整体并发症发生率和死亡率居高不下,使得该技术在中毒领域的临床应用步履维艰,仅见于极少数绝望情况下的尝试。此阶段最具代表性的案例是1989年报道的首例维拉帕米中毒应用[12](见表 1),尽管治疗最终失败,但其大胆实践为后续研究积累了宝贵经验,深刻揭示了ECMO在中毒救治领域的潜力与早期技术局限。
2.2 临床认知深化与适应证拓展期(20世纪90年代至21世纪初)随着氧合器材料和泵技术经历了显著的革新,同时伴随临床实践经验的系统性积累,ECMO在急性中毒治疗领域的应用呈现稳步增长态势[13],治疗效果也有了一定程度的提升。其临床应用开始从单纯的心肺复苏扩展至可逆性中毒所致的心源性休克和难治性呼吸衰竭。1991年McVey与Corke成功应用ECMO救治普萘洛尔过量患者[14],标志着ECMO正式成为中毒救治领域一种可行的二线救援手段。此后,临床报道逐渐增多,适应证从心血管药物(如钙通道阻滞剂、β受体阻滞剂)拓展至三环类抗抑郁药、镇静安眠药等。此阶段的核心特征体现为从治疗可行性评估向适用对象选择的转变,临床医生据此筛选毒物效应可逆、常规治疗无效且不伴有不可逆损伤的潜在生存者。然而,证据多源于病例报告或小系列病例,缺乏系统性总结,ECMO的启动时机、管理模式和疗效预测仍主要依赖于个体化经验。
2.3 技术集成与系统化应用期(2010年至今)进入21世纪第二个十年,ECMO技术迎来革命性进步。聚甲基戊烯[poly(4-methyl-1-pentene), PMP]膜氧合器因其卓越的气体交换效率和长效性成为主流,离心泵的普及和小型化设备(如Cardiohelp便携式体外膜肺氧合系统)的出现极大地提升了救治的便携性和效率。更为重要的是,ECMO不再被视作孤立的支持技术,而是深度集成到中毒救治的多模态体系中,尤其是与连续性肾脏替代治疗(continuous renal replacement therapy, CRRT)的联合[15-16],实现了“支持”与“清除”的协同,为缓解中毒性多器官功能衰竭(multiple organ dysfunction syndrome, MODS)提供了新策略。中国体外生命支持登记数据显示(2017—2021年)[17],中毒患者ECMO使用率持续上升,其中农业毒物与药物中毒占据主要范畴,印证了其在中国的快速发展。当前的研究焦点已从“是否可用”转变为如何优化,即精准把握上机时机、制定个体化抗凝方案、管理并发症以及建立科学的撤离策略。
3 ECMO在急性中毒领域应用的最新进展 3.1 临床应用拓展与技术精准化近年来,ECMO在急性中毒领域的应用呈现出显著的范式转变,其焦点已从治疗可行性的探讨,集中于应用方案的优化。其成功应用的核心在于严格把握一个基本原则:ECMO适用于毒物效应可逆,但常规治疗无法维持生命,以致患者无法存活至毒物自行代谢清除的情况[10]。它并非直接解毒,而是为机体自身的代谢和恢复争取宝贵的“时间窗” [9]。
3.1.1 启动ECMO的总体适应证与决策路径对于急性中毒患者,启动ECMO支持的决策应基于全面的临床评估,其核心指征包括:(1)顽固性心源性休克[18]:尽管进行了充分的液体复苏和高剂量血管活性药物支持,仍持续存在低血压(平均动脉压 < 65 mmHg,1 mmHg=0.133 kPa)和组织低灌注(如乳酸持续升高)。(2)难治性呼吸衰竭[19]:在优化机械通气(包括肺保护性通气策略、高呼气末正压(positive end-expiratory pressure, PEEP)、甚至俯卧位通气)后,仍存在严重低氧血症或危及生命的高碳酸血症。(3)心脏骤停[20]:中毒相关的心脏骤停,尤其是对常规高级生命支持(advanced cardiovascular life support, ACLS)无反应或自主循环(return of spontaneous circulation, ROSC)难以维持者,可考虑体外心肺复苏(extracorporeal cardiopulmonary resuscitation, ECPR)。(4)可逆性评估[21]:必须有合理预期认为中毒导致的功能障碍在得到一段时间支持后是可逆的,且不存在严重的不可逆性脑损伤或其他终末期疾病。
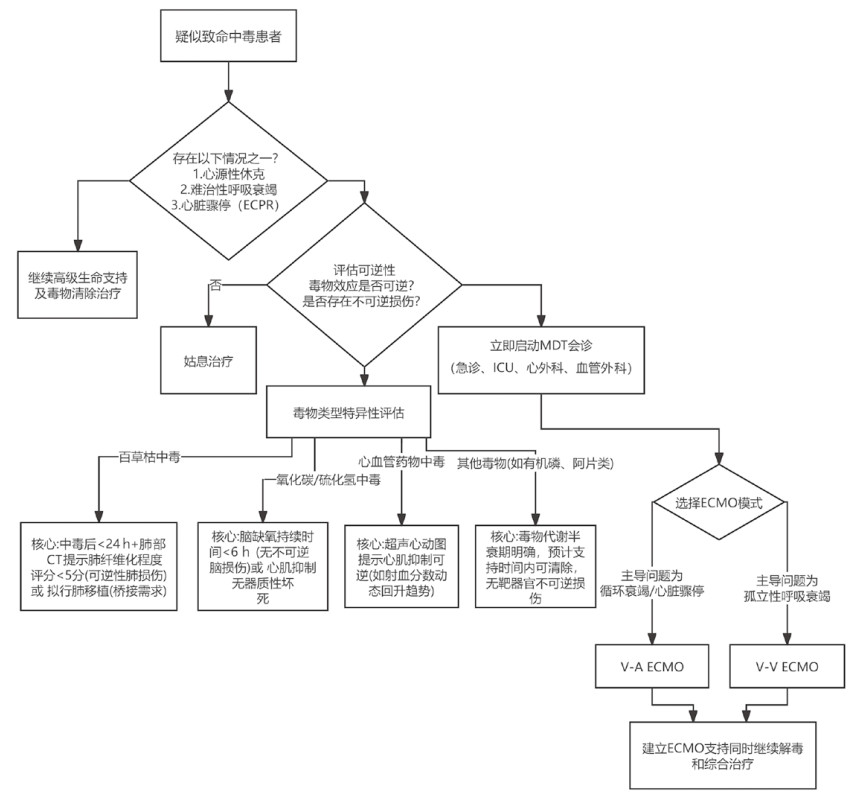
综上,急性中毒患者启动ECMO的决策是一个快速、综合的评估过程。为便于临床医生快速掌握其核心要点,基于现有证据和临床经验,总结了以下推荐决策路径(图 1),本路径强调了生命体征的顽固性、常规治疗的无反应性以及潜在的可逆性是启动ECMO支持的三大核心依据。
|
| 注:ECMO为体外膜肺氧合,V-A ECMO为静脉-动脉体外膜肺氧合,V-V ECMO为静脉-静脉体外膜肺氧合,ECPR为体外心肺复苏,CT为电子计算机断层扫描,MDT为多学科团队协作,ICU为重症监护病房;图中决策路径依据正文3.1.1节所述适应证 图 1 急性中毒患者ECMO支持临床决策推荐 |
|
|
不同毒物作用的靶器官不同,因此ECMO的模式选择和治疗策略需个体化精准选择(表 2)。
| 中毒类型 | 病理生理变化 | 推荐ECMO模式 | 介入时机与考量 | 疗效与证据强度 | 参考文献 |
| 心血管药物 | 心肌抑制、心源性休克 | V-A ECMO | 出现难治性低血压或休克,对高剂量血管活性药无反应,是公认的救命措施 | 生存率59%~63.6%[9, 22],证据较强,有多项队列研究支持 | [9, 22-24] |
| 百草枯 | 早期急性肺损伤,后期不可逆肺纤维化 | V-V ECMO (主要为肺移植桥接) | 争议巨大。仅在极早期、预计为可逆性肺损伤或作为肺移植桥接时考虑。需严格筛选 | 生存率约40%[25-26],甚至更低;多为病例系列,预后差,伦理争议突出 | [16, 25-28] |
| 磷化铝 | 暴发性心肌炎、心源性休克 | V-A ECMO | 出现严重心力衰竭的早期迹象时积极介入,是生存的关键 | 生存率可达50%以上[29-30],病例报告显示能有效逆转心衰 | [26, 29-31] |
| 一氧化碳/硫化氢 | 组织缺氧、心肌抑制、心脏骤停 | V-A/V-V (依主导表现而定) | V-A用于心脏骤停或心源性休克;V-V用于严重低氧血症;ECPR(ECMO辅助复苏)优势明显 | 生存率良好(硫化氢报道可达100%)[32-33],是ECPR的良好适应证 | [7, 32-34] |
| 毒品/镇静剂(如阿片类) | 呼吸抑制、低氧性心脏骤停 | V-A/V-V | 用于常规复苏无效的心脏骤停或严重呼吸衰竭;毒物代谢后功能多可恢复,预后较好 | 生存率显著优于常规复苏[35];多项研究支持其在ECPR中的应用 | [35] |
| 注:ECMO为体外膜肺氧合,V-A ECMO为静脉-动脉体外膜肺氧合,V-V ECMO为静脉-静脉体外膜肺氧合,ECPR为体外心肺复苏 | |||||
ECMO的疗效源于其双重机制:一是直接的心肺功能替代支持,维持生命体征;二是通过维持有效循环和氧供,增强机体代谢和自身清除能力,间接促进毒物消除[36-37]。基于此机制,其应用已从经典的心血管药物中毒,从而拓展到其他的中毒领域。
农药中毒除表 2所列外,在严格筛选下,ECMO也可用于有机磷中毒所致的难治性呼吸衰竭[38]。除此之外,敌草快是一种剧毒除草剂,大剂量摄入可导致多器官功能衰竭,死亡率极高。在临床实践中,对于出现严重呼吸循环衰竭的敌草快中毒患者,ECMO能够提供有效的呼吸和循环支持[39]。但是在百草枯中毒中,其预后极差,ECMO的使用存在重大伦理争议[25, 40-41]。争议焦点主要集中于两方面:①ECMO是否可能延长无意义的生命存活,而非改善最终生存质量;②在医疗资源有限的情况下,将高成本支持技术用于预后极差的患者,其资源分配的合理性值得深思。因此,临床决策必须审慎,并与患者家属就成功率、经济负担及潜在结局进行充分、透明的沟通。其应用仅应在高度选择性的病例中考虑,例如:患者极其年轻、摄入剂量不确定但早期即出现严重低氧血症、或作为肺移植的桥接。必须与家属充分沟通其极低的成功率和高昂的经济代价。同时儿童中毒患者应用ECMO需根据体重和体表面积选择专用套包和管路,管理参数需精细化调整。证据多来源于个案,但总体原则与成人相似[42]。
ECMO气体中毒中的应用除用于表 2中的硫化氢和一氧化碳。其在光气中毒中的应用也已得到广泛报道。在一项研究中,纳入了4例因光气中毒而导致重度急性呼吸窘迫综合征(acute respiratory distress syndrome, ARDS)患者的治疗数据,研究发现早期应用ECMO可显著改善患者的氧合状态,消除体内潴留的二氧化碳,减少呼吸机相关的肺损伤,且所有患者最终预后良好[43]。汞蒸气作为ARDS的罕见致病因素,其临床治疗策略尚未明确。尽管ECMO技术已成功应用于部分毒物性肺损伤的救治,但针对汞蒸气吸入所致肺损伤的早期干预方案及远期预后管理,目前仍缺乏系统性研究数据。典型临床案例研究显示[44],针对重症汞蒸气吸入性肺损伤患者,采用静脉-静脉体外膜肺氧合(vein-vein extracorporeal membrane oxygenation, V-V ECMO)联合糖皮质激素与双重螯合剂治疗方案,不仅实现肺功能完全逆转,且未出现典型神经毒性及肾毒性并发症,这一发现从临床实践层面证实了V-V ECMO在汞蒸气致ARDS治疗中的关键作用。随着ECMO技术的普及,其在各种刺激性气体中毒中的应用也逐渐扩大,相关临床案例数量不断增加[45]。
在毒蛇咬伤中,某些毒蛇的毒液含有多种毒素,可导致患者出现凝血功能障碍、呼吸肌麻痹、心脏毒性等严重并发症,甚至危及生命。对于出现严重呼吸循环衰竭的毒蛇咬伤中毒患者,ECMO能够提供有效的呼吸和循环支持,同时结合抗蛇毒血清等治疗措施。在最新的研究中,已有发现通过人工智能从头设计出能有效中和蛇毒中剧毒成分的蛋白质,为开发更安全、有效、经济且易获取的抗蛇毒疗法带来新希望[46]。然而,关于ECMO在毒蛇咬伤中的应用,相关研究和病例报告较为匮乏。尽管如此,随着研究深入,其在毒蛇咬伤中毒的应用前景值得期待。
3.1.3 儿童急性中毒ECMO应用要点儿童中毒患者应用ECMO时,还需重点关注其与成人的管理差异。①抗凝方案:儿童肝素剂量需依据体表面积精确计算,并更频繁监测抗凝指标[47-48]。②上机时机:由于儿童生理代偿能力有限,对严重中毒的耐受性更差,ECMO介入指征可相对放宽,避免等待至终末期[42]。③管理参数:需针对儿童心血管与呼吸系统特点进行精细化调整[42]。
3.2 技术改进与创新 3.2.1 氧合器ECMO技术在急性中毒领域的应用经历了显著的技术进步与创新,这些进步为急性中毒患者的救治带来了新的希望。在氧合器方面,新型材料的应用显著提升了其性能。传统的硅橡胶膜氧合器逐渐被替代,更先进的PMP膜氧合器使用频率越来越高。PMP膜作为典型的非疏水性材料,具有优异的生物相容性,显著降低了凝血和血栓发生的风险,血栓发生率降低30%[49]。此外,一项近期的研究表明,通过含氟共价有机框架(fluorinated covalent organic framework, FCOF)纳米纤维与PMP混合所制成的一种混合膜,具有更好的血液相容性和氧合性能。其中,PMP-FCOF-3中空纤维膜的氧气交换率约为309.8 mL/(min·m2),比商业PMP中空纤维膜高出77.3%,该结果基于体外血液模拟实验(n=3),临床转化效果仍需验证;二氧化碳交换率约为251.7 mL/(min·m2),与商业PMP中空纤维膜相当[50]。这种改进使得ECMO在急性中毒导致的呼吸衰竭治疗中,能够更迅速、有效地改善患者的氧合状态,减轻肺部的负担,为患者的后期康复创造更好的条件。临床研究表明[51],PMP膜氧气传输率显著高于聚丙烯(polypropylene, PP)膜,同时其更换率更低,而PP膜只能作为紧急情况下的一种替代方案。此外,通过两性离子聚合物和多巴胺的共沉积方法, 来改变PMP膜表面的物理化学性质,可显著降低其蛋白质吸附量,延长凝血时间,从而进一步提升氧合器的血液相容性和气体交换性能[52],为ECMO在急性中毒引起的严重呼吸衰竭治疗中的应用提供了新的思路。
3.2.2 小型化ECMO设备与离心泵智能化小型化ECMO设备的出现开创了ECMO治疗的新时代,其主要特点是其便携性和多功能性显著提升[53]。在面对中毒引起的心脏骤停等紧急情况时,小型化设备能够快速部署至患者床边。目前市场上已出现多种小型化ECMO设备,其中Cardiohelp设备作为一种代表性的便携ECMO设备,可提供ECMO和心室辅助设备(ventricular assist device, VAD)双重支持,并具有良好的运输性,能够便捷地在医院内转运。此外,Novalung系统作为一种专为新生儿、婴儿及儿童设计的小型化ECMO系统,其精确的流量控制和氧合性能对新生儿护理具有重要意义[53-54]。与此同时,离心泵技术的智能化发展为ECMO治疗带来了新的突破[55],并且已初步融入人工智能技术,例如通过机器学习算法实时分析血流动力学数据,实现泵速的自适应调整,为精准控制支持强度提供了新途径。这为未来构建更完善的AI辅助决策系统奠定了技术基础。智能化离心泵配备了先进的控制系统,能够实时监测并反馈血液流量、压力等关键参数,并根据患者病情动态调整泵速和流量,从而实现更精准的治疗效果。然而,关于滚压泵与离心泵的对比研究表明,离心泵在ECMO应用中展现出显著的优势,包括减少血液传输时间、提高患者转运便利性等,但其可能伴随着非手术部位出血风险的增加等潜在安全性问题[56]。但新型生物涂层离心泵可减少出血风险[56]。因此,进一步的研究仍需深入探讨离心泵对凝血功能的影响。对于急性中毒患者的转运管理而言,中毒患者常需进行电子计算机断层扫描(computed tomography, CT)等影像学检查以评估脑、肺等器官损伤,或在ECMO建立前已位于急诊抢救室。设备小型化使得ECMO能进行院前部署和标准护理配备[57],也确保了检查治疗过程中的支持不间断,为明确诊断和综合处理提供了可能。小型化设备能使院内转运的时间缩短40%。同时,智能化的离心泵能够根据患者转运过程中动态变化的生理参数,实时调整运行参数,从而保证ECMO治疗的连续性和稳定性,为急性中毒患者的临床救治提供了更高效的支持方案。
3.2.3 抗凝管理在急性中毒患者的ECMO治疗过程中,抗凝管理是至关重要的关键环节[58]。为了实现精准的抗凝管理,近年来一些新型抗凝监测设备及方式被成功应用于急性中毒患者的ECMO治疗中。这些监测手段能够及时发现患者凝血功能的异常变化,从而为临床医护人员提供重要的指导依据,帮助其及时调整抗凝药物的剂量,避免因抗凝管理不当而引发的严重并发症。研究[59]表明,通过活化凝血时间(activated clotting time, ACT)标准化监测流程对ECMO患者的肝素抗凝进行动态监测和优化,可以使患者的凝血程度达到最佳状态,从而有效降低出血不良情况的发生率,血栓弹力图(thromboelastography, TEG)联合ACT监测可进一步优化肝素剂量。同时,有研究[60]强调在ECMO治疗中,应综合运用多种实验室检测手段,制定个性化的抗凝方案,以确保治疗效果的最大化和患者安全性,这在急性中毒患者的ECMO治疗中同样适用。体外生命支持组织(Extracorporeal Life Support Organization, ELSO)发布的成人及儿童ECMO回路管理指南中,对抗凝策略、监测指标及并发症处理提供了系统推荐,为临床实践提供了重要依据[47]。
上述技术创新显著提升了ECMO在中毒救治中的安全性和效率,为临床应用拓展奠定基础。
3.3 ECMO与其他治疗方式的联合应用近年来,ECMO联合血液净化技术的创新性应用为重度中毒患者提供了新的治疗可能性。在ECMO系统建立后,血液净化装置可串联于膜肺后(血流量维持300~400 mL/min),利用体外循环的稳定血流实现持续净化。CRRT与ECMO的联合应用可协同清除白细胞介素-6(interleukin-6, IL-6)、肿瘤坏死因子-α(tumor necrosis factor-α, TNF-α)等炎症介质,其协同机制主要体现在以下两方面:ECMO通过提供稳定的血流动力学支持,为CRRT的顺利实施创造了必要条件;而CRRT可高效清除中小分子溶质及炎症因子(如IL-6降幅达50%以上[61]),从而有效遏制“细胞因子风暴”,减轻过度炎症反应对组织器官的损伤。这一联合策略通过血流动力学管理与炎症调控的双重机制,显著改善危重症患者的病理生理状态。研究表明这种联合模式能够有效抑制全身炎症反应,改善重症肺炎及其他重症患者的预后,并显著提高他们的生存率[62-64]。目前,ECMO联合血液净化治疗在药物中毒的救治中应用广泛,其适应证范围涵盖心血管类和镇静催眠等药物诱导的心源性休克患者,以及刺激性气体中毒所致急性呼吸功能衰竭患者等多种类型[16]。在蘑菇中毒患者中,也有研究报告指出通过ECMO和血液净化治疗显著提高了患者的救治率[65]。磷化铝中毒由于缺乏有效的解毒剂,常常伴随高病死率且可能导致心脏骤停。在一项相关研究中,患者在常规治疗无效后,及时启动ECMO及CRRT治疗,并联合其他综合治疗,能够在ECMO支持下稳定呼吸和循环功能,同时通过血液净化技术清除体内毒素。治疗后,患者的炎症因子水平显著下降,多器官功能障碍得到改善,最终好转出院[66]。这种联合治疗模式在重度乙二醇中毒患者中的应用也已得到报道,充分体现了其在急性中毒领域的重要价值[67]。ECMO联合血液净化技术通过维持多器官功能,降低脓毒症和多器官功能衰竭综合征(multiple organ dysfunction syndrome, MODS)的发生风险,显著改善了危重中毒患者的预后。临床实践已证实,这种联合治疗方案在多种急性中毒和危重症患者中均取得了良好效果,突破了传统治疗的局限性,通过体外生命支持与血液净化的空间协同、时间序贯,显著提升了患者的生存率和长期预后。
静脉注射脂质乳剂(intravenous lipid emulsion, ILE)作为一种潜在的中毒解毒疗法,已应用于多种局麻药物中毒的临床处置[68]。然而,ECMO治疗期间应用ILE的安全性始终存疑,主要归因于循环管路凝血及脂质聚集的潜在风险。前期体外研究显示[69],即使实施规范化肝素抗凝,ECMO管路中仍可观测到脂质分层与聚集现象,并可能诱发管路凝血,值得注意的是,ECMO与ILE联合应用时,脂质沉积量呈现显著减少趋势,但前提是在规范化肝素抗凝的基础上,并维持较高的血流速度(通常建议≥300 mL/min)。若未满足这些条件,脂质聚集和管路凝血的风险依然显著。因此对于常规治疗无效的致命性脂溶性药物中毒,在充分权衡利弊后,仍可考虑在ECMO支持下使用ILE。使用期间需格外密切地监测ECMO管路、膜肺和滤器(如果同时有CRRT)的跨膜压差,警惕血栓形成的早期迹象。鉴于ECMO治疗中ILE使用频率相对较低,系统性临床数据存在显著缺失,导致该联合疗法的临床适应证范围及潜在不良反应尚未得到充分阐明,并不推荐作为常规方案,决策需非常谨慎。
4 局限性尽管ECMO在急性中毒救治中已取得显著进展,其临床应用仍存在若干局限。
4.1 循证证据不足现有研究多为单中心个案报告或小样本队列(如磷化铝中毒生存率数据来自单中心个案[66]),缺乏多中心随机对照试验(multicenter randomized controlled trial, RCT)验证疗效优势,部分适应证(如百草枯中毒[16, 25-28])推荐级别低。
4.2 罕见中毒证据匮乏ECMO在部分罕见中毒(如蛇毒)中的应用证据多基于个案报告[70],样本量有限且缺乏系统性研究支持,导致在该类中毒救治中临床医生难以依据充分证据制定标准化治疗方案,临床决策往往依赖于经验而非循证医学依据。
4.3 抗凝管理无专用指南抗凝管理方面尚缺乏针对中毒患者的专用指南。不同类型中毒对凝血功能的影响存在差异,然而目前仍无专门指导中毒患者在ECMO治疗期间抗凝管理的规范,这使临床工作者在权衡抗凝治疗收益与出血风险时面临较大不确定性,从而增加了治疗风险[48]。
4.4 成本与技术门槛高ECMO高昂的治疗成本与技术复杂性也限制了其在基层医疗机构的推广。设备购置、维护及耗材费用均较为昂贵,同时该技术需依托专业团队进行操作与管理,导致其在基层医疗环境中的成本效益比较低,普及程度有限,进而影响患者获得及时救治的机会[40]。
5 未来与展望近年来,ECMO因其独特的脏器支持优势在急性中毒领域展现出显著临床价值。随着医疗技术的革新与多学科协作模式的深化,ECMO正逐步突破传统应用边界,在急性中毒救治领域呈现多维发展态势。
5.1 技术研发与创新未来ECMO系统的优化应聚焦于材料学、流体力学和智能控制技术的融合创新。研发具有仿生内皮涂层的新型氧合器及管路[71],有望显著降低血栓形成风险,减少抗凝药物依赖,尤其适用于凝血功能紊乱的中毒患者。离心泵的智能化升级应注重实时自适应调控能力,结合血流动力学与代谢指标动态调整支持强度,提升治疗的个体化水平。此外,便携式、一体化ECMO设备的开发将有助于提高院前及基层医疗单位的应急救治能力,缩短ECMO支持的时间延迟。
5.2 精准化临床决策与预警系统构建建立中毒特异性ECMO预警与决策支持系统是未来的重要方向。建议整合毒物种类、暴露剂量、乳酸水平、序贯器官衰竭评分(sequential organ failure assessment, SOFA)、器官功能动态变化等多维参数,构建预测模型与临床路径,辅助医生更早识别ECMO适应证、把握最佳干预时机。尤其对于百草枯、磷化铝等高致死性毒物,需明确ECMO介入的临界指标和退出标准,避免无效支持。人工智能与机器学习技术在数据处理、模式识别和实时预警方面具有广阔应用前景,可协助实现ECMO治疗的动态优化与风险管控[41]。
5.3 多学科协作与整合治疗模式ECMO在中毒救治中的高效实施离不开急诊医学、重症医学、毒理学、心血管内科、输血科及护理团队的多学科协作(multidisciplinary team, MDT)。未来应推动建立区域中毒救治ECMO支持中心,形成快速响应网络和标准化转运流程。同时,深化ECMO与其他体外治疗技术的整合,如联合CRRT、血浆置换、血液灌流等多模式净化策略,实现“支持+清除”协同治疗,尤其适用于合并多器官功能障碍的严重中毒病例。
5.4 循证医学研究与临床转化目前ECMO在中毒领域的应用仍缺乏高级别临床证据[13]。未来应积极开展多中心、前瞻性队列研究,尤其聚焦于不同毒物类型的中毒人群,明确ECMO治疗的生存获益群体、最佳支持模式和管理策略。建立中毒ECMO病例登记数据库,进行长期随访和疗效评估,为指南制定提供依据。同时,加强基础与转化研究,探索ECMO干预对毒物代谢、炎症反应及器官修复的机制,为临床实践提供理论支撑。
5.5 基层推广与卫生经济学评估ECMO技术的高成本及复杂性仍是制约其广泛开展的重要因素。未来应通过模拟培训、远程会诊和技术下沉提升基层医院ECMO团队的建设水平。同时,开展卫生经济学评价,明确ECMO在中毒救治中的成本效益比,为医保政策及资源分配提供数据支持,推动这一救命技术在更广泛范围内合理应用。
综上所述,ECMO在急性中毒领域的应用已取得了显著的进展,通过不断的技术创新、临床实践与多学科协作,ECMO将在急性中毒治疗中发挥更加重要的作用,为急性中毒患者带来更多的生存希望与更好的预后。
利益冲突 所有作者声明无利益冲突
| [1] | Liu SF, Ling LJ, Ma J, et al. Trends and profiles of acute poisoning cases: a retrospective analysis[J]. Front Public Health, 2023, 11: 1235304. DOI:10.3389/fpubh.2023.1235304 |
| [2] | Salem W, Abdulrouf P, Thomas B, et al. Epidemiology, clinical characteristics, and associated cost of acute poisoning: a retrospective study[J]. J Pharm Policy Pract, 2024, 17(1): 2325513. DOI:10.1080/20523211.2024.2325513 |
| [3] | 高艳霞, 孙同文. 中国急性中毒十年研究回顾与展望[J]. 中华急诊医学杂志, 2023, 32(3): 282-287. DOI:10.3760/cma.j.issn.1671-0282.2023.03.002 |
| [4] | White A, Fan E. What is ECMO?[J]. Am J Respir Crit Care Med, 2016, 193(6): 9-10. DOI:10.1164/rccm.1936P9 |
| [5] | 王伟, 靳有鹏. 体外膜肺氧合在急性中毒救治中的应用[J]. 中国小儿急救医学, 2024, 31(9): 690-693. DOI:10.3760/cma.j.issn.1673-4912.2024.09.010 |
| [6] | Greenberg K, Kohl B. ECMO used successfully in a near fatal case of opioid-induced acute respiratory distress syndrome[J]. Am J Emerg Med, 2018, 36(2): 343. DOI:10.1016/j.ajem.2017.11.020 |
| [7] | Teerapuncharoen K, Sharma NS, Barker AB, et al. Successful treatment of severe carbon monoxide poisoning and refractory shock using extracorporeal membrane oxygenation[J]. Respir Care, 2015, 60(9): e155-e160. DOI:10.4187/respcare.03990 |
| [8] | Simonsen C, Magnusdottir SO, Andreasen JJ, et al. ECMO improves survival following cardiogenic shock due to carbon monoxide poisoning - an experimental porcine model[J]. Scand J Trauma Resusc Emerg Med, 2018, 26(1): 103. DOI:10.1186/s13049-018-0570-6 |
| [9] | Weiner L, Mazzeffi MA, Hines EQ, et al. Clinical utility of venoarterial-extracorporeal membrane oxygenation (VA-ECMO) in patients with drug-induced cardiogenic shock: a retrospective study of the Extracorporeal Life Support Organizations' ECMO case registry[J]. Clin Toxicol, 2020, 58(7): 705-710. DOI:10.1080/15563650.2019.1676896 |
| [10] | 蒋敏, 王军, 何飞. ECMO技术对急性中毒导致心搏骤停的治疗进展[J]. 中华危重病急救医学, 2020, 32(9): 1145-1148. DOI:10.3760/cma.j.cn121430-20200608-00445 |
| [11] | Freedman MD, Gal J, Freed CR. Extracorporeal pump assistance: novel treatment for acute lidocaine poisoning[J]. Eur J Clin Pharmacol, 1982, 22(2): 129-135. DOI:10.1007/BF00542457 |
| [12] | Hendren WG, Schieber RS, Garrettson LK. Extracorporeal bypass for the treatment of verapamil poisoning[J]. Ann Emerg Med, 1989, 18(9): 984-987. DOI:10.1016/s0196-0644(89)80465-2 |
| [13] | Upchurch C, Blumenberg A, Brodie D, et al. Extracorporeal membrane oxygenation use in poisoning: a narrative review with clinical recommendations[J]. Clin Toxicol, 2021, 59(10): 877-887. DOI:10.1080/15563650.2021.1945082 |
| [14] | McVey FK, Corke CF. Extracorporeal circulation in the management of massive propranolol overdose[J]. Anaesthesia, 1991, 46(9): 744-746. DOI:10.1111/j.1365-2044.1991.tb09770.x |
| [15] | Dang XT, Lv SZ, Huang M, et al. Extracorporeal multi-organ support: ECMO, CRRT, and hemoperfusion for acute alcohol intoxication with renal and respiratory failure[J]. Ren Fail, 2025, 47(1): 2487211. DOI:10.1080/0886022X.2025.2487211 |
| [16] | 张云, 王群文, 高霏, 等. 体外膜肺氧合联合血液净化技术在药物中毒或过量救治中应用的文献分析[J]. 中国中西医结合急救杂志, 2021, 38(5): 584-589. DOI:10.3969/j.issn.1008-9691.2021.05.016 |
| [17] | 辛萌, 谢海秀, 杜中涛, 等. 体外膜肺氧合在中国急性中毒成人患者中的应用: 2017—2021年体外生命支持登记的回顾性分析[J]. 中华急诊医学杂志, 2022, 31(12): 1597-1602. DOI:10.3760/cma.j.issn.1671-0282.2022.12.004 |
| [18] | Trieu NHK, Pham HM, Huynh DQ, et al. Peripheral VA-ECMO: from evolving indications to perioperative implications[J]. Anesthesiol Perioper Sci, 2025, 3(2): 26. DOI:10.1007/s44254-025-00106-5 |
| [19] | Kim HS, Kim JH, Chung CR, et al. Lung compliance and outcomes in patients with acute respiratory distress syndrome receiving ECMO[J]. Ann Thorac Surg, 2019, 108(1): 176-182. DOI:10.1016/j.athoracsur.2019.01.055 |
| [20] | Ng M, Wong ZY, Ponampalam R. Extracorporeal cardio-pulmonary resuscitation in poisoning: a scoping review article[J]. Resusc Plus, 2023, 13: 100367. DOI:10.1016/j.resplu.2023.100367 |
| [21] | Gupta V, Wander GS. ECMO in poisoning[J]. J Card Crit Care, 2017, 1(2): 82-88. DOI:10.1055/s-0038-1626679 |
| [22] | Friedrichson B, Jasny T, Old O, et al. Extracorporeal membrane oxygenation in cardiovascular medication poisoning. A German-wide retrospective study[J]. Sci Rep, 2024, 14(1): 21761. DOI:10.1038/s41598-024-72547-0 |
| [23] | Brunet J, Valette X, Ivascau C, et al. Extracorporeal life support for refractory cardiac arrest or shock: a 10-year study[J]. ASAIO J, 2015, 61(6): 676-681. DOI:10.1097/MAT.0000000000000282 |
| [24] | Ramanathan K, Tan CS, Rycus P, et al. Extracorporeal membrane oxygenation for poisoning in adult patients: outcomes and predictors of mortality[J]. Intensive Care Med, 2017, 43(10): 1538-1539. DOI:10.1007/s00134-017-4842-9 |
| [25] | Feng MX, Lu YQ. Performance of extracorporeal membrane oxygenation in patients with fatal paraquat poisoning: grasp for straws?[J]. World J Emerg Med, 2021, 12(3): 232-234. DOI:10.5847/wjem.j.1920-8642.2021.03.013 |
| [26] | 张云, 张晶, 高霏, 等. ECMO在农药中毒救治中的应用[J]. 中国急救复苏与灾害医学杂志, 2020, 15(12): 1466-1470. DOI:10.3969/j.issn.1673-6966.2020.12.036 |
| [27] | Ali Usman A, Spelde AE, Lutfi W, et al. Percutaneous venopulmonary extracorporeal membrane oxygenation as bridge to lung transplantation[J]. ASAIO J, 2024, 70(9): 758-766. DOI:10.1097/MAT.0000000000002179 |
| [28] | Jiao GH, Li XN, Wu B, et al. Case report: delayed lung transplantation with intraoperative ECMO support for herbicide intoxication-related irreversible pulmonary fibrosis: strategy and outcome[J]. Front Surg, 2021, 8: 754816. DOI:10.3389/fsurg.2021.754816 |
| [29] | 张倩, 芦雨, 谢永鹏, 等. VA-ECMO成功逆转口服磷化铝所致的急性心力衰竭1例[J]. 中国急救复苏与灾害医学杂志, 2023, 18(11): 1534-1536. DOI:10.3969/j.issn.1673-6966.2023.11.031 |
| [30] | Moshiri M, Dorooshi G, Etemad L, et al. Effect of extracorporeal membrane oxygenation on mortality rate of aluminum phosphate poisoning: a systematic review and meta-analysis[J]. J Res Med Sci, 2024, 29: 62. DOI:10.4103/jrms.jrms_123_24 |
| [31] | Mehra A, Sharma N. ECMO: a ray of hope for young suicide victims with acute aluminum phosphide poisoning and shock[J]. Indian Heart J, 2016, 68(3): 256-257. DOI:10.1016/j.ihj.2016.02.006 |
| [32] | 葛文汉, 石岩, 李梦秋, 等. 体外膜肺氧合治疗急性重度硫化氢中毒3例[J]. 中华急诊医学杂志, 2024, 33(3): 395-397. DOI:10.3760/cma.j.issn.1671-0282.2024.03.023 |
| [33] | Berg Hansen K, Christensen S, Birkelund T, et al. Prolonged cardiogenic shock due to hydrogen sulfide intoxication requiring long-term venoarterial extracorporeal membrane support[J]. JACC Case Rep, 2022, 4(21): 1389-1393. DOI:10.1016/j.jaccas.2022.05.035 |
| [34] | Dun Y, Zhang XL, Pan L, et al. Extracorporeal membrane oxygenation for acute toxic inhalations: case reports and literature review[J]. Front Med, 2021, 8: 745555. DOI:10.3389/fmed.2021.745555 |
| [35] | Cole JB, Olives TD, Ulici A, et al. Extracorporeal membrane oxygenation for poisonings reported to U.S. poison centers from 2000 to 2018: an analysis of the national poison data system[J]. Crit Care Med, 2020, 48(8): 1111-1119. DOI:10.1097/CCM.0000000000004401 |
| [36] | Squiers JJ, Lima B, DiMaio JM. Contemporary extracorporeal membrane oxygenation therapy in adults: Fundamental principles and systematic review of the evidence[J]. J Thorac Cardiovasc Surg, 2016, 152(1): 20-32. DOI:10.1016/j.jtcvs.2016.02.067 |
| [37] | Torre DE, Mangino D, Pirri C. Veno-arterial extracorporeal membrane oxygenation in cardiotoxic drug-induced cardiogenic shock: a systematic narrative review[J]. Life, 2025, 15(6): 925. DOI:10.3390/life15060925 |
| [38] | Suermondt C, de Marcellus C, Vodovar D, et al. Successful ECMO rescue for organophosphate poisoning causing refractory acute respiratory distress syndrome: a first pediatric case[J]. Arch Pediatr, 2025, 32(6): 423-426. DOI:10.1016/j.arcped.2025.05.001 |
| [39] | 急性敌草快中毒诊断与治疗专家共识组. 急性敌草快中毒诊断与治疗专家共识[J]. 中华急诊医学杂志, 2020, 29(10): 1282-1289. DOI:10.3760/cma.j.issn.1671-0282.2020.10.002 |
| [40] | Kichloo A, Kumar A, Amir R, et al. Utilization of extracorporeal membrane oxygenation during the COVID-19 pandemic[J]. World J Crit Care Med, 2021, 10(1): 1-11. DOI:10.5492/wjccm.v10.i1.1 |
| [41] | Chen SS, Liu LJ, Hu DJ, et al. Effect of artificial intelligence in extracorporeal membrane oxygenation: a systematic review and meta-analysis[J]. Intensive Crit Care Nurs, 2026, 92: 104165. DOI:10.1016/j.iccn.2025.104165 |
| [42] | Rambaud J, Barbaro RP, MacRae DJ, et al. Extracorporeal membrane oxygenation in pediatric acute respiratory distress syndrome: from the second pediatric acute lung injury consensus conference[J]. Pediatr Crit Care Med, 2023, 24. DOI:10.1097/PCC.0000000000003164 |
| [43] | 何招辉, 杨小刚, 杨春丽. ECMO治疗急性光气中毒致急性呼吸窘迫综合征: 附4例报告[J]. 中华危重病急救医学, 2019, 31(2): 232-235. DOI:10.3760/cma.j.issn.2095-4352.2019.02.022 |
| [44] | Zambratto J, Gottesman E, Hasan Z, et al. Extracorporeal membrane oxygenation in the treatment of acute elemental mercury inhalation toxicity[J]. Chest, 2025, 167(3): e71-e74. DOI:10.1016/j.chest.2024.09.043 |
| [45] | 叶纪录, 濮雪华. ECMO救治有机氟中毒病例报道[J]. 中华急诊医学杂志, 2019, 28(10): 1326-1328. DOI:10.3760/cma.j.issn.1671-0282.2019.10.0230 |
| [46] | Vázquez Torres S, Benard Valle M, Mackessy SP, et al. De novo designed proteins neutralize lethal snake venom toxins[J]. Nature, 2025, 639(8053): 225-231. DOI:10.1038/s41586-024-08393-x |
| [47] | Gajkowski EF, Herrera G, Hatton L, et al. ELSO guidelines for adult and pediatric extracorporeal membrane oxygenation circuits[J]. ASAIO J, 2022, 68(2): 133-152. DOI:10.1097/MAT.0000000000001630 |
| [48] | Burša F, Sklienka P, Frelich M, et al. Anticoagulation management during extracorporeal membrane oxygenation-a mini-review[J]. Medicina, 2022, 58(12): 1783. DOI:10.3390/medicina58121783 |
| [49] | 张海彬, 张良震, 黄斯珉, 等. 人工膜肺氧合器技术进展[J]. 安徽工业大学学报(自然科学版), 2023, 40(3): 288-296. DOI:10.12415/j.issn.1671-7872.23030 |
| [50] | Guo YH, Yang G, Yu SY, et al. Engineering fluorinated COF-based hybrid membranes for efficient blood oxygenation[J]. J Membr Sci, 2025, 721: 123815. DOI:10.1016/j.memsci.2025.123815 |
| [51] | Valenzuela-Faccini N, Poveda-Henao C, Flórez-Navas C, et al. Outcomes of ECMO support with polypropylene membrane during pandemic times: a retrospective cohort study[J]. BMC Pulm Med, 2024, 24(1): 41. DOI:10.1186/s12890-023-02753-5 |
| [52] | He T, Wang XY, Sun ZY, et al. Improvement hemocompatibility of antithrombotic PMP hollow fiber membranes based on the modification of zwitterionic polymer in ECMO application[J]. J Membr Sci, 2024, 704: 122891. DOI:10.1016/j.memsci.2024.122891 |
| [53] | Nwanna-Nzewunwa O, Keshavamurthy S. ECMO – current applications, technological advances and future directions[M]//FIRSTENBERG M S. Evolving therapies and technologies in extracorporeal membrane oxygenation. Rijeka: IntechOpen. 2024. |
| [54] | MacLaren G, Combes A, Bartlett RH. Contemporary extracorporeal membrane oxygenation for adult respiratory failure: life support in the new era[J]. Intensive Care Med, 2012, 38(2): 210-220. DOI:10.1007/s00134-011-2439-2 |
| [55] | Glomp G, Cortelli M, Bernicker B, et al. Open-access smart blood pump platform for controlling extracorporeal membrane oxygenation[J]. HardwareX, 2025, 22: e00644. DOI:10.1016/j.ohx.2025.e00644 |
| [56] | Halaweish I, Cole A, Cooley E, et al. Roller and centrifugal pumps: a retrospective comparison of bleeding complications in extracorporeal membrane oxygenation[J]. ASAIO J, 2015, 61(5): 496-501. DOI:10.1097/MAT.0000000000000243 |
| [57] | Kapoor MC. ECMO-augmented resuscitation: redefining refractory cardiac arrest management[J]. J Resusc, 2025, 2(1): 1-3. DOI:10.4103/ircf.ircf_5_25 |
| [58] | 赵举, 崔勇丽, 刘刚. ECMO中的抗凝管理[J]. 中国急救医学, 2021, 41(7): 607-609. DOI:10.3969/j.issn.1002-1949.2021.07.015 |
| [59] | 魏玲. ACT标准化监测流程在ECMO患者肝素抗凝中的应用研究[J]. 中国当代医药, 2021, 28(35) 47-49, 53. DOI:10.3969/j.issn.1674-4721.2021.35.013 |
| [60] | Rodrigues AB, Rodrigues A, Correia CJ, et al. Anticoagulation management in V-V ECMO patients: a multidisciplinary pragmatic protocol[J]. J Clin Med, 2024, 13(3): 719. DOI:10.3390/jcm13030719 |
| [61] | Barbura N, Porosnicu TM, Papurica M, et al. Continuous hemofiltration during extracorporeal membrane oxygenation in adult septic shock: a comparative cohort analysis[J]. Biomedicines, 2025, 13(8): 1829. DOI:10.3390/biomedicines13081829 |
| [62] | 郑丽, 牟春英, 黎巧玲. 1例重症肺炎患者体外膜肺氧合联合连续性肾脏替代及机械通气治疗的康复护理[J]. 现代临床护理, 2021, 20(9): 81-85. DOI:10.3969/j.issn.1671-8283.2021.9.015 |
| [63] | Awori Hayanga JW, Song TE, Durham L, et al. Extracorporeal hemoadsorption in critically ill COVID-19 patients on VV ECMO: the CytoSorb therapy in COVID-19 (CTC) registry[J]. Crit Care, 2023, 27(1): 243. DOI:10.1186/s13054-023-04517-3 |
| [64] | Ronco C, Bagshaw SM, Bellomo R, et al. Extracorporeal blood purification and organ support in the critically ill patient during COVID-19 pandemic: expert review and recommendation[J]. Blood Purif, 2021, 50(1): 17-27. DOI:10.1159/000508125 |
| [65] | 伍琪, 吴姝玲, 上官美琴, 等. 1例蘑菇中毒患者体外心肺复苏联合血液净化救治的护理[J]. 天津护理, 2021, 29(5): 598-601. DOI:10.3969/j.issn.1006-9143.2021.05.026 |
| [66] | 雷容, 岳朝辅, 刘世盛, 等. 体外膜肺氧合联合血液净化抢救磷化铝中毒致心搏呼吸骤停1例[J]. 中华急诊医学杂志, 2024, 33(3): 403-405. DOI:10.3760/cma.j.issn.1671-0282.2024.03.026 |
| [67] | 潘勇莉, 吕世进, 蒋镇宏. 静脉-静脉体外膜肺氧合联合血液净化成功救治重度乙二醇中毒1例[J]. 中华劳动卫生职业病杂志, 2022, 40(12): 947-949. DOI:10.3760/cma.j.cn121094-20220303-00106 |
| [68] | Bilvanisi S, Gülen M, Sabak M, et al. Intravenous lipid emulsion therapy in drug overdose and poisoning: an updated review[J]. Eurasian J Med, 2024, 56(3): 205-212. DOI:10.5152/eurasianjmed.2024.24510 |
| [69] | Sin JH, Tom A, Toyoda A, et al. High-dose intravenous lipid emulsion affecting successful initiation of continuous venovenous hemofiltration and extracorporeal membrane oxygenation[J]. Clin Toxicol, 2018, 56(2): 149-150. DOI:10.1080/15563650.2017.1341633 |
| [70] | Pooboni SK. ECMO in tropical diseases[J]. Egypt J Crit Care Med, 2018, 6(3): 101-102. DOI:10.1016/j.ejccm.2018.12.003 |
| [71] | Hagiwara J, DellaVolpe JD, Matsuzaki Y. What are the best biocompatible materials for extracorporeal membrane oxygenation[J]. J Funct Biomater, 2025, 16(6): 226. DOI:10.3390/jfb16060226 |
 2026, Vol. 35
2026, Vol. 35