脑卒中(stroke)是全球公共卫生领域面临的一项重大挑战,以其高发病率、高致残率和高死亡率持续威胁着人类的健康。根据《柳叶刀》2021年发布的全球疾病负担研究中脑卒中负担及其风险因素分析,脑卒中已成为继缺血性心脏病和COVID-19之后的第三大死亡原因。而在所有新发卒中病例中,缺血性脑卒中占比最大(780万,占比65.3%)[1],其造成的神经功能缺损与社会经济负担尤为严峻。在我国,卒中同样对经济发展与卫生健康造成了极大的负担。自2008年ECASS Ⅲ(European Cooperative Acute Stroke Study Ⅲ)试验[2]将静脉溶栓时间窗扩展至4.5 h以来,传统静脉溶栓的时间窗被限定为发病后4.5 h内。但临床实践中仍存在许多急性缺血性脑卒中(acute ischemic stroke, AIS)患者因就诊延迟或发病时间不明的卒中(unknown onset stroke, UOS)等原因超过了该时间窗而不能得到及时有效的治疗。于是,以“组织窗”代替“时间窗”的概念被提出[3],通过精准的影像学进行个体化的筛选,更多超时间窗患者将获得再灌注治疗的机会。超时间窗静脉溶栓成为AIS治疗研究探索的新方向,影像技术与传统和新型药物的双重驱动正推动着静脉溶栓治疗从单纯根据时间窗的“一刀切”模式转变向通过影像筛选的个体化新范式。
1 阿替普酶和替奈普酶 1.1 阿替普酶作为第二代溶栓剂,自1995年NINDS试验(National Institute of Neurological Disorders and Stroke)[4]取得突破性成果以来,阿替普酶(alteplase, rt-PA)在发病3 h内的AIS的治疗中的地位被确认,并成为了标准治疗方案。此后,ECASS Ⅲ试验[2]进一步将治疗时间窗扩展至4.5 h,使更多患者得到了治疗的机会,并为后续的超时间窗溶栓研究奠定了基础。尽管阿替普酶已作为目前急性缺血性卒中的标准治疗药物,但仍存在一些缺点,包括:易受纤溶酶原激活剂抑制剂-1(PAI-1)影响,导致酶活性快速丧失;半衰期短暂(约4~5 min),需要较大剂量单次治疗及持续输注;主要在纤维蛋白表面发挥作用,血栓穿透能力有限,可能延迟血流再通并增加血管再闭风险;会激活基质金属蛋白酶,破坏血脑屏障,进而引发脑出血和脑水肿等[5]。但不可否认的是,相较于尿激酶(urokinase, uPA)、链激酶(streptokinase, SK)等第一代非特异性纤溶剂,阿替普酶作为目前的一线标准药物,对血栓内纤维蛋白的靶向作用使其更具治疗选择性并降低了出血风险,显著提高了AIS患者的治疗效果,为缺血性脑卒中的治疗作出了卓越的贡献。
1.2 替奈普酶替奈普酶(tenecteplase, TNK)是一种新型的溶栓药物,是天然组织型纤溶酶原激活剂分子的一种变体,其纤维蛋白特异性比阿替普酶高14倍,具有更长的半衰期、较慢的血浆清除速度,并且对PAI-1的抗性比阿替普酶强80倍,其约18 min的半衰期允许单次推注给药[6-7]。同属第三代溶栓药的瑞替普酶需两次给药,且存在靶向性较弱、出血风险较高的问题[8],相比之下,替奈普酶成为指南优先推荐的方案。
多项临床试验都证明了替奈普酶的安全性与有效性并不劣于阿替普酶[9-11],并且可能改善临床结局[12]。一项大型回顾性多中心研究表明,相较于阿替普酶,替奈普酶带来了更低的死亡率和更少的出血并发症[13]。2023年欧洲卒中组织(ESO)的快速推荐文件也指出,替奈普酶在AIS治疗中是一种安全有效的选择,替奈普酶0.25 mg/kg是一种合理的阿替普酶替代药物[14]。2025年3月3日,美国食品药品监督管理局(Food and Drug Administration, FDA)已批准替奈普酶(商品名:TNKase)用于治疗成人AIS,这是近30年来继阿替普酶后FDA批准的首个卒中药物,这一批准基于AcT试验(Alteplase compared to Tenecteplase)[10]的结果,该研究为替奈普酶在急性缺血性脑卒中治疗中的标准化应用提供了关键证据。替奈普酶凭借其药效学和药代动力的优势与潜在延长治疗窗的特性,已被多项指南推荐用于AIS,为急性缺血性脑卒中治疗带来了新的希望。
2 缺血性脑卒中超时间窗的个体化溶栓必要性在急性缺血性脑卒中(acute ischemic stroke, AIS)的救治中,“时间就是大脑”(Time is brain)的理念始终贯穿临床决策。研究显示,未经治疗的大血管闭塞性卒中患者每min将损失190万个神经元、138亿个突触及12 km长度的轴突纤维[15],而在静脉溶栓(intravenous thrombolysis, IVT)中每缩短1 min的DNT(door-to-needle time)平均可额外延长1.8 d的额外健康寿命,在静脉注射t-PA治疗过程中节省的几分钟时间便能为患者带来显著临床获益[16]。可见,静脉溶栓在AIS的救治中时间扮演着极其重要的角色,然而存在部分患者因治疗延误而超过了传统时间窗。此外,还有约1/3的患者为UOS患者[17],UOS可分为醒后卒中(wake-up stroke, WUS)和非醒后未目击卒中(non-wake-up unwitnessed stroke, NWUS)[18],其中WUS约占急性缺血性卒中的14%~25%[19-21],这进一步限制了患者获得再灌注治疗的机会。因此,延长溶栓时间窗的研究十分重要,这可以使更多患者得到接受治疗的机会。1981年缺血半暗带的概念被正式提出[22],此后,随着神经影像学的不断发展,基于神经影像学的选择方法使更多的卒中患者可受益于时间窗后的再灌注治疗,这主要基于通过影像学识别可挽救的缺血半暗带与不可逆损伤的缺血核心[23-24]。研究显示,即便在超出了传统时间窗的未接受治疗患者群体中,良好的侧支循环与更大范围的半暗带挽救、更少的梗死进展呈现相关性[25],及时的再灌注可以挽救缺血半暗带。同时,脑组织缺血性损伤的进展在个体间存在差异[26],这受到侧支循环的充分性、血压、代谢环境、温度和患者年龄等因素影响[27],部分患者的缺血半暗带组织在超出现有时间窗后仍可能存活。因此,AIS患者的救治不应该单纯根据传统时间窗进行判断,而应该尽可能地筛选出可以通过溶栓获益的患者。“晚期时间窗悖论”(late window paradox)研究的提出进一步挑战了传统认知:多项随机对照试验(如DAWN、DEFUSE 3)证实,经影像筛选的超时间窗患者接受管内治疗(endovascular therapy, EVT)后,其功能预后甚至可能优于早期治疗组[28]。这种现象挑战了传统的“时间就是大脑”的观念,强调了影像学评估在急性缺血性脑卒中治疗中的重要性。虽然卒中发作时间对于治疗的重要性不容忽视,但神经影像学对缺血性卒中患者的个体化评估为扩大溶栓治疗的适用范围提供了希望。尽管EVT技术的发展显著提升了大血管闭塞患者的疗效,并可通过影像学的筛选将时间窗扩展至24 h[29],但其应用受到医疗资源分布、技术门槛和适应症筛选的限制。静脉溶栓治疗凭借其快速给药、低技术门槛以及广泛的适用性,仍然是许多患者的重要治疗选择[30],尤其是非大血管闭塞患者。
3 影像学指导的个体化溶栓 3.1 多模态影像超时间窗AIS患者的溶栓决策对影像评估提出双重要求:一方面需快速排除出血禁忌,另一方面需精准识别存活脑组织。影像学为缺血性脑卒的诊断与治疗提供了关键信息,从排除出血、定位责任病灶到量化可挽救脑组织,多模态影像学技术贯穿缺血性脑卒中诊疗全流程,在制定个体化再灌注策略中起到决策作用。目前进行的超时间窗溶栓研究中,对患者进行成像筛选的方法主要依赖于CT灌注(computed tomography perfusion, CTP)核心/半暗带不匹配、磁共振灌注-弥散不匹配(PWI-DWI mismatch)或弥散加权成像与液体衰减反转恢复序列不匹配(DWI-FLAIR mismatch)[31-32],也是目前指南中推荐的影像筛选标准[33],然而,对于那些不符合特定试验纳入标准的患者,是否适合接受溶栓治疗仍存在诸多不确定性。此外,多模态影像技术在基层医疗场景中的可及性仍存在显著局限。
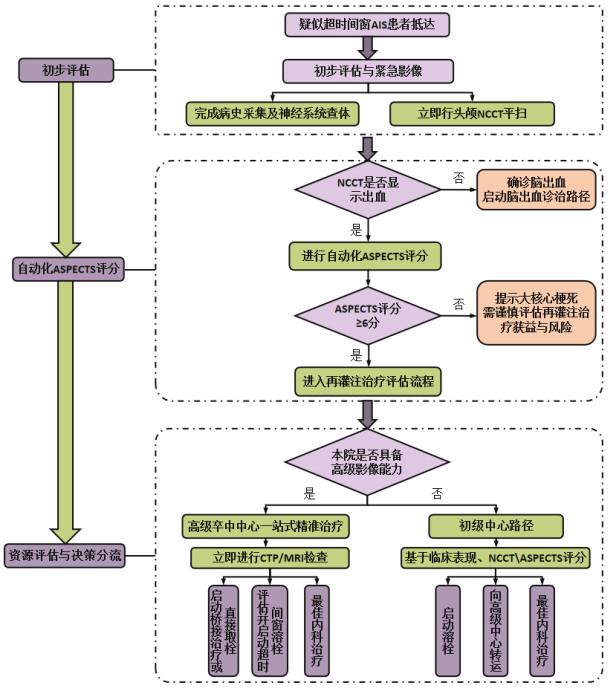
3.2 非增强CT非增强CT(non-contrast computed tomography, NCCT)通常用于排除出血,其对缺血半暗带的识别与对侧支循环的评估能力有限,然而,对于广大的初级卒中中心或基层医院,NCCT是普遍可及且快速的技术。CT血管成像(computed tomography angiography, CTA)可直观显示大血管闭塞,设备普及率日益增高,但其对缺血核心和半暗带的评估能力有限。CTP和MRI成像虽能精准量化缺血核心与半暗带,但对设备、技术、后处理软件及专业人员要求高,扫描与后处理耗时较长,在多数基层医院难以常规开展。阿尔伯塔省卒中项目早期CT评分(Alberta Stroke Program Early CT Score, ASPECTS)[34]可系统性量化评估CT的缺血改变,能够快速识别那些已经出现广泛、不可逆早期梗死征象的患者,目前普遍将ASPECTS评分≥6分作为筛选可溶栓获益的安全标准[35-36],是功能结局和症状性出血的预测因子。但由于主观性差异的问题,不同的评分者得出的结果可能不同[37],然而随着算法的进步,自动化的ASPECTS可以解决这一问题[38-39]。研究表明基于NCCT的自动化ASPECTS评分与参考标准达的一致性相当,同时和CTP定义的梗死核心存在中等程度的相关性[40]。基于自动化ASPECTS评分的筛选只需常规NCCT扫描,且不受主观差异与误判的影响,在排除高风险溶栓患者的同时,可快速辅助决策启动静脉溶栓或向高级中心转诊(图 1), 对于超时间窗急性缺血性脑卒中患者的早期分流与个体化管理具有临床指导意义。目前,指南并不推荐对仅完成NCCT检查未见颅内出血的醒后或发病时间不明的急性缺血性卒中患者使用替奈普酶进行静脉溶栓治疗[33]。在TWIST试验[41]中,使用了NCCT选择症状识别后4.5 h内的醒来卒中患者,但并未显示出基于NCCT的选择可以带来更好的功能结局。因此,只依赖NCCT和ASPECTS评分加上临床的判断是否能够为超时间窗患者带来益处仍有待进一步研究,以期在基层场景中能够使更多患者获益。
|
| 图 1 超时间窗AIS患者基于自动化ASPECTS评分急诊影像评估与决策路径 |
|
|
为了缩短患者从发病到溶栓的时间,2003年移动卒中单元(mobile stroke unit, MSU)概念被正式提出[42],在移动救护车内配备小型可移动CT、急救器械、药品及专业医护团队,以实现“上车即溶栓”。随着MSU的使用,患者者获得优良预后的概率提升了约65%,且使发病至IVT的时间缩短30 min[43]。但CT只能用于排除脑出血,而对于超时间窗或醒后卒中的患者溶栓的指导意义有限。2024年我国学者提出在急诊卒中场景下建立急诊卒中单元(emergency stroke unit, ESU),并配备0.23 T低场强可移动核磁设备[44],以实现卒中患者入院后一站式处理,缩短DNT。通过扫描DWI、FLAIR序列和专门开发的血肿增强反转恢复(hematoma enhanced inversion recovery, HEIR)序列,鉴别AIS与脑出血[45],且可通过DWI-FLAIR不匹配对醒后卒中患者进行及时的溶栓。与CT相比,其可以直接显示病灶,做出更精准的决策。低场强MRI与标准3.0 T固定MRI相比具有较好的一致性[46],且更加简单快速,适用场景更加丰富且不避金属,在对于基层医院也更加可及。
4 超时间窗溶栓应用研究进展 4.1 阿替普酶在超时间窗溶栓中的应用近年来,多项高质量随机临床试验为阿替普酶超时间窗应用提供了关键证据。WAKE-UP试验[31]针对醒后卒中/发病时间不明患者,通过MRI-DWI/FLAIR不匹配筛选,证实发病9 h内溶栓可显著改善90 d功能预后(mRS 0-1, OR=1.61),且未显著增加sICH风险(2.0% vs. 0.4%)。在WAKE-UP试验结果公布后,三项正在进行的试验(EXTEND、ECASS-4和THAWS)提前终止。EXTEND试验[32]进一步将筛选标准扩展至CTP或MRI成像,得出了4.5~9.0 h时间窗内阿替普酶治疗仍可获益(OR=1.86)的结果,尽管sICH发生率有所上升(5.3%)。而ECASS-4[47]试验和THAWS[48]试验的结果未发现使用阿替普酶可使患者获益。这些研究共同推动了指南更新,但影像技术的复杂性与出血风险仍是临床决策的权衡重点。
在将阿替普酶的溶栓时间窗扩展到9 h的基础上,最新的多项研究进一步挑战了静脉溶栓的时间窗限制,旨探索在进一步拓宽治疗时间窗的获益与风险。2024年发表的HOPE试验[49]旨在研究脑卒中发生后4.5~24 h CTP显示存在潜在可抢救组织的AIS患者是否能够获益于静脉溶栓。HOPE试验进一步扩大了阿替普酶溶栓的研究时间窗,该试验仍在进行阶段,这可能进一步突破阿替普酶治疗的时间限制,覆盖更多因就诊延迟或医疗资源不足而无法接受治疗的患者。2025年Yan等[50]首次证实后循环卒中在4.5~24 h超时间窗内溶栓可改善功能预后,且安全性可控。这一结果提示,后循环卒中的可救治时间窗可能较前循环更宽,与其侧支循环丰富、缺血耐受性较强有关,进一步丰富了阿替普酶在超时间窗溶栓应用的研究。
阿替普酶作为目前AIS溶栓治疗的核心标准药物,随着影像学技术的进步和临床研究的深入,超时间窗溶栓的探索为部分患者提供了新的治疗可能,相应的荟萃分析也证实了其可以使患者得到更好的结局[51],并可以预见后循环梗死与醒后卒中患者可能从更灵活的时间窗中获益,但仍需审慎权衡获益与风险,未来需要更多的研究来进一步证实其安全性并指定更加标准的筛选与治疗标准。
4.2 替奈普酶在在超时间窗溶栓中的应用在时间窗内溶栓安全性的上,替奈普酶凭借对纤维蛋白的更高的亲和力,能够更精准地靶向血栓;对PAI-1的更高的抵抗性,有助于减少全身纤溶状态;更长的半衰期,使其可以单次快速静脉推注给药,减少了治疗的延误,展现出了在超时间窗溶栓中的潜能,吸引了更多学者对于其在超时间窗溶栓的使用中的探索。
一项2024年发表的TRACE Ⅲ试验[52]旨在评估在发病(包括醒后和无目击者卒中)4.5~24 h内并且前循环大动脉闭塞但无法进行血管内治疗的卒中患者中使用替奈普酶(0.25 mg/kg,最大25 mg)静脉溶栓对比标准药物治疗的有效性和安全性。该实验得出发病后4.5~24 h内前循环大动脉闭塞的且有影像半暗带的急性缺血性卒中患者,替奈普酶组在90 d时的mRS评分≤1的比例显著高于标准药物治疗组(33.0% vs. 24.2%, P=0.03),且在次要终点如90 d mRS分布、早期神经功能改善、24 h再灌注率等方面,替奈普酶组均明显高于对照组。该试验为发病4.5~24 h且无法接受血管内治疗的颅内大血管闭塞脑卒中患者提供了重要的治疗选择。而另一项名为TIMELESS的研究[53],纳入发病后4.5~24 h内的急性缺血性脑卒中患者,且通过灌注成像筛选,该试验未能显示出替奈普酶的显著疗效,这可能与TIMELESS研究中机械取栓的高比例(77.3%)与使用替奈普酶静脉溶栓到动脉穿刺的中位时间较短(15 min)有关,TIMELESS的阴性结果提示,在血管内治疗可立即实施且桥接时间极短的医疗环境下,替奈普酶的总体附加效应有限,这可能是血管内治疗本身极高的再通成功率掩盖了溶栓的效应差别。但其亚组分析揭示了一个重要的信号:在大脑中动脉M1段闭塞的患者中,替奈普酶组的功能独立率较安慰剂组显著更高(45.9% vs. 31.4%; aOR=2.03, 95%CI: 1.14~3.66)。这提示,即使在高比例血管内治疗的背景下,特定具有大血栓负荷的闭塞类型患者,仍可能从桥接静脉溶栓中获得额外益处。这一发现与TRACE Ⅲ的总体阳性结果形成了互补而非对立:TRACE Ⅲ回答了在无EVT场景下替奈普酶的价值;而TIMELESS的亚组分析则提示,在EVT可用的背景下,基于闭塞部位等特征进行精细化选择,替奈普酶仍可能使患者获益。此外,患者的人群分布、潜在的卒中病因以及更精细的影像学表现也可能进一步细化受益人群。可以预见的是,替奈普酶在延长溶栓时间窗的应用中存在着有效性与可行性,还需要更多的研究进一步证实并推进。2025年发表的CHABLIS-T Ⅱ试验[54]也为替奈普酶在超时间窗(4.5~24 h)AIS患者中的应用提供了重要证据,表明替奈普酶可以显著提高再灌注率且不增加症状性出血风险,但对患者90 d的功能预后影响有限。该试验结果支持在大/中血管闭塞所致AIS的特定患者群体中使用替奈普酶进行静脉溶栓治疗,尤其是在无法及时进行血管内治疗的情况下。然而,试验的局限性包括样本量较小和可能存在选择偏差,未来仍需更大规模的试验来进一步验证这些发现。2025年发布的一项ETERNAL-LVO试验设计[55],评估替奈普酶对症状出现后24 h内出现的大血管闭塞患者的益处。该试验基于目前替奈普酶在 > 4.5 h时间窗内的证据,进一步评估替奈普酶在有血管内治疗机会但可能延迟或需要从初级卒中中心转移到综合卒中中心的患者中的疗效,其结果将广泛适用于“滴定和运输”患者以及那些延迟接受血管内治疗的患者。相对于TRACE Ⅲ试验中无法获得血管内治疗的患者群体与TIMELESS试验中能够快速获得血管内治疗的患者群体,该试验可以填补替奈普酶在可获得延迟血管内治疗的患者群体中研究,随着该试验的进行,可以进一步丰富替奈普酶在超时间窗溶栓治疗中的研究,推动其在超时间溶栓中的应用,对血管内治疗资源分配的可及性的问题也可提参考。
可以预见,随着更多研究的进行,AIS患者的救治将逐步脱离时间的限制,替奈普酶在超时间窗溶栓中的应用也将逐步提上日程。但不可否认的是,当前,替奈普酶在超时间窗溶栓的应用中还存在着亟待解决的问题,包括在时间窗内及超时间窗应用中的最佳剂量的问题,是否出现导致症状性脑出血概率较高的问题等。
5 总结与展望上述试验逐步推动着指南的更新[14, 33, 56], 在急性缺血性脑卒中超时间窗患者的个体化静脉溶栓治疗领域的研究和应用都取得了显著进展,由此,可以预见在特定患者中延长溶栓时间窗的更多可能性以及新型溶栓药物的潜力。然而,仍有许多问题需要解决,包括如何更准确地筛选适合溶栓治疗的患者、如何在缺乏多模态影像的场景中筛选患者、如何进一步提高治疗的安全性和有效性等,需要更多高质量的前瞻性临床研究来进一步确认超时间窗溶栓治疗中最佳应用方案。一项DEFUSE 3试验的事后分析显示[57],对于发病24 h仍存在缺血半暗带的患者,依然可能从超晚时间窗(> 24 h)的血管内治疗中获益。这提示对于发病超过24 h的患者,不应轻易排除再灌注治疗的可能性,而应个体化地评估其脑组织的缺血状态,也给了我们探索静脉溶栓更长时间窗的启发。通过不断的研究和实践,今后有望为急性缺血性脑卒中超时间窗患者提供更精准、更有效的个体化静脉溶栓治疗方案,降低卒中的致残率和死亡率,改善患者的预后。
利益冲突 所有作者声明无利益冲突
| [1] | GBD 2021 Stroke Risk Factor Collaborators. Global, regional, and national burden of stroke and its risk factors, 1990-2021:a systematic analysis for the Global Burden of Disease Study 2021[J]. Lancet Neurol, 2024, 23(10): 973-1003. DOI:10.1016/S1474-4422(24)00369-7 |
| [2] | Hacke W, Kaste M, Bluhmki E, et al. Thrombolysis with alteplase 3 to 4.5 hours after acute ischemic stroke[J]. N Engl J Med, 2008, 359(13): 1317-1329. DOI:10.1056/NEJMoa0804656 |
| [3] | Hacke W. A new DAWN for imaging-based selection in the treatment of acute stroke[J]. N Engl J Med, 2018, 378(1): 81-83. DOI:10.1056/NEJMe1713367 |
| [4] | National Institute of Neurological Disorders and Stroke rt-PA Stroke Study Group. Tissue plasminogen activator for acute ischemic stroke[J]. N Engl J Med, 1995, 333(24): 1581-1587. DOI:10.1056/NEJM199512143332401 |
| [5] | 孔维麟, 杨清武. 急性缺血性卒中溶栓药物的研究进展[J]. 中国药房, 2023, 34(4): 497-501. DOI:10.6039/j.issn.1001-0408.2023.04.22 |
| [6] | Keyt BA, Paoni NF, Refino CJ, et al. A faster-acting and more potent form of tissue plasminogen activator[J]. Proc Natl Acad Sci USA, 1994, 91(9): 3670-3674. DOI:10.1073/pnas.91.9.3670 |
| [7] | Davydov L, Cheng JWM. Tenecteplase: a review[J]. Clin Ther, 2001, 23(7): 982-997. DOI:10.1016/S0149-2918(01)80086-2 |
| [8] | Li SY, Gu HQ, Li H, et al. Reteplase versus alteplase for acute ischemic stroke[J]. N Engl J Med, 2024, 390(24): 2264-2273. DOI:10.1056/NEJMoa2400314 |
| [9] | Wang YJ, Li SY, Pan YS, et al. Tenecteplase versus alteplase in acute ischaemic cerebrovascular events (TRACE-2): a phase 3, multicentre, open-label, randomised controlled, non-inferiority trial[J]. Lancet, 2023, 401(10377): 645-654. DOI:10.1016/S0140-6736(22)02600-9 |
| [10] | Menon BK, Buck BH, Singh N, et al. Intravenous tenecteplase compared with alteplase for acute ischaemic stroke in Canada (AcT): a pragmatic, multicentre, open-label, registry-linked, randomised, controlled, non-inferiority trial[J]. Lancet, 2022, 400(10347): 161-169. DOI:10.1016/S0140-6736(22)01054-6 |
| [11] | Meng X, Li SY, Dai HG, et al. Tenecteplase vs alteplase for patients with acute ischemic stroke: the ORIGINAL randomized clinical trial[J]. JAMA, 2024, 332(17): 1437-1445. DOI:10.1001/jama.2024.14721 |
| [12] | Campbell BCV, Mitchell PJ, Churilov L, et al. Tenecteplase versus alteplase before thrombectomy for ischemic stroke[J]. N Engl J Med, 2018, 378(17): 1573-1582. DOI:10.1056/NEJMoa1716405 |
| [13] | Murphy LR, Hill TP, Paul K, et al. Tenecteplase versus alteplase for acute stroke: mortality and bleeding complications[J]. Ann Emerg Med, 2023, 82(6): 720-728. DOI:10.1016/j.annemergmed.2023.03.022 |
| [14] | Alamowitch S, Turc G, Palaiodimou L, et al. European Stroke Organisation (ESO) expedited recommendation on tenecteplase for acute ischaemic stroke[J]. Eur Stroke J, 2023, 8(1): 8-54. DOI:10.1177/23969873221150022 |
| [15] | Saver JL. Time is brain: quantified[J]. Stroke, 2006, 37(1): 263-266. DOI:10.1161/01.str.0000196957.55928.ab |
| [16] | Meretoja A, Keshtkaran M, Saver JL, et al. Stroke thrombolysis: save a minute, save a day[J]. Stroke, 2014, 45(4): 1053-1058. DOI:10.1161/STROKEAHA.113.002910 |
| [17] | Kim YJ, Kim BJ, Kwon SU, et al. Unclear-onset stroke: Daytime-unwitnessed stroke vs. wake-up stroke[J]. Int J Stroke, 2016, 11(2): 212-220. DOI:10.1177/1747493015616513 |
| [18] | Kamogawa N, Miwa K, Toyoda K, et al. Thrombolysis for wake-up stroke versus non-wake-up unwitnessed stroke: EOS individual patient data meta-analysis[J]. Stroke, 2024, 55(4): 895-904. DOI:10.1161/STROKEAHA.123.043358 |
| [19] | Sun T, Xu Z, Diao SS, et al. Safety and cost-effectiveness thrombolysis by diffusion-weighted imaging and fluid attenuated inversion recovery mismatch for wake-up stroke[J]. Clin Neurol Neurosurg, 2018, 170: 47-52. DOI:10.1016/j.clineuro.2018.04.027 |
| [20] | MacKey J, Kleindorfer D, Sucharew H, et al. Population-based study of wake-up strokes[J]. Neurology, 2011, 76(19): 1662-1667. DOI:10.1212/WNL.0b013e318219fb30 |
| [21] | Serena J, Dávalos A, Segura T, et al. Stroke on awakening: looking for a more rational management[J]. Cerebrovasc Dis, 2003, 16(2): 128-133. DOI:10.1159/000070592 |
| [22] | Astrup J, Siesjö BK, Symon L. Thresholds in cerebral ischemia-the ischemic penumbra[J]. Stroke, 1981, 12(6): 723-725. DOI:10.1161/01.str.12.6.723 |
| [23] | Ermine CM, Bivard A, Parsons MW, et al. The ischemic penumbra: From concept to reality[J]. Int J Stroke, 2021, 16(5): 497-509. DOI:10.1177/1747493020975229 |
| [24] | Seners P, Yuen N, Mlynash M, et al. Quantification of penumbral volume in association with time from stroke onset in acute ischemic stroke with large vessel occlusion[J]. JAMA Neurol, 2023, 80(5): 523-528. DOI:10.1001/jamaneurol.2023.0265 |
| [25] | Vagal A, Aviv R, Sucharew H, et al. Collateral clock is more important than time clock for tissue fate[J]. Stroke, 2018, 49(9): 2102-2107. DOI:10.1161/STROKEAHA.118.021484 |
| [26] | Wheeler HM, Mlynash M, Inoue M, et al. The growth rate of early DWI lesions is highly variable and associated with penumbral salvage and clinical outcomes following endovascular reperfusion[J]. Int J Stroke, 2015, 10(5): 723-729. DOI:10.1111/ijs.12436 |
| [27] | Moskowitz MA, Lo EH, Iadecola C. The science of stroke: mechanisms in search of treatments[J]. Neuron, 2010, 67(2): 181-198. DOI:10.1016/j.neuron.2010.07.002 |
| [28] | Albers GW. Late window paradox[J]. Stroke, 2018, 49(3): 768-771. DOI:10.1161/strokeaha.117.020200 |
| [29] | Nogueira RG, Jadhav AP, Haussen DC, et al. Thrombectomy 6 to 24 hours after stroke with a mismatch between deficit and infarct[J]. N Engl J Med, 2018, 378(1): 11-21. DOI:10.1056/NEJMoa1706442 |
| [30] | Aguiar de Sousa D, Wilkie A, Norrving B, et al. Delivery of acute ischaemic stroke treatments in the European region in 2019 and 2020[J]. Eur Stroke J, 2023, 8(3): 618-628. DOI:10.1177/23969873231186042 |
| [31] | Thomalla G, Simonsen CZ, Boutitie F, et al. MRI-guided thrombolysis for stroke with unknown time of onset[J]. N Engl J Med, 2018, 379(7): 611-622. DOI:10.1056/NEJMoa1804355 |
| [32] | Ma H, Campbell BCV, Parsons MW, et al. Thrombolysis guided by perfusion imaging up to 9 hours after onset of stroke[J]. N Engl J Med, 2019, 380(19): 1795-1803. DOI:10.1056/NEJMoa1813046 |
| [33] | 中国卒中学会, 《中国卒中学会急性缺血性卒中再灌注治疗指南》编写组. 中国卒中学会急性缺血性卒中再灌注治疗指南2024[J]. 中国卒中杂志, 2024, 19(12): 1460-1478. DOI:10.3969/j.issn.1673-5765.2024.12.014 |
| [34] | Barber PA, Demchuk AM, Zhang J, et al. Validity and reliability of a quantitative computed tomography score in predicting outcome of hyperacute stroke before thrombolytic therapy. ASPECTS Study Group. Alberta Stroke Programme Early CT Score[J]. Lancet, 2000, 355(9216): 1670-1674. DOI:10.1016/s0140-6736(00)02237-6 |
| [35] | GOYAL M, DEMCHUK A M, MENON B K, et al. Randomized assessment of rapid endovascular treatment of ischemic stroke[J]. N Engl J Med, 2015, 372(11): 1019-30. DOI:10.1056/NEJMoa1414905 |
| [36] | FUGATE J E, BRINJIKJI W, CLOFT H, et al. Variability of stroke patients meeting endovascular stroke trial criteria in a non-clinical trial setting[J]. J Neuroradiol, 2018, 45(3): 192-5. DOI:10.1016/j.neurad.2017.11.003 |
| [37] | van Horn N, Kniep H, Broocks G, et al. ASPECTS interobserver agreement of 100 investigators from the TENSION study[J]. Clin Neuroradiol, 2021, 31(4): 1093-1100. DOI:10.1007/s00062-020-00988-x |
| [38] | Maegerlein C, Fischer J, Mönch S, et al. Automated calculation of the Alberta stroke program early CT score: feasibility and reliability[J]. Radiology, 2019, 291(1): 141-148. DOI:10.1148/radiol.2019181228 |
| [39] | Sundaram VK, Goldstein J, Wheelwright D, et al. Automated ASPECTS in acute ischemic stroke: a comparative analysis with CT perfusion[J]. AJNR Am J Neuroradiol, 2019, 40(12): 2033-2038. DOI:10.3174/ajnr.A6303 |
| [40] | Chen XY, Lin SS, Zhang XX, et al. Prognosis with non-contrast CT and CT Perfusion imaging in thrombolysis-treated acute ischemic stroke[J]. Eur J Radiol, 2022, 149: 110217. DOI:10.1016/j.ejrad.2022.110217 |
| [41] | Roaldsen MB, Eltoft A, Wilsgaard T, et al. Safety and efficacy of tenecteplase in patients with wake-up stroke assessed by non-contrast CT (TWIST): a multicentre, open-label, randomised controlled trial[J]. Lancet Neurol, 2023, 22(2): 117-126. DOI:10.1016/S1474-4422(22)00484-7 |
| [42] | Fassbender K, Walter S, Liu Y, et al. "Mobile stroke unit" for hyperacute stroke treatment[J]. Stroke, 2003, 34(6): e44. DOI:10.1161/01.str.0000075573.22885.3b |
| [43] | Turc G, Hadziahmetovic M, Walter S, et al. Comparison of mobile stroke unit with usual care for acute ischemic stroke management: a systematic review and meta-analysis[J]. JAMA Neurol, 2022, 79(3): 281-290. DOI:10.1001/jamaneurol.2021.5321 |
| [44] | 中国卒中学会急诊卒中单元联盟. 急诊卒中单元建设指南[J]. 中国卒中杂志, 2024, 19(12): 1454-1459. DOI:10.3969/j.issn.1673-5765.2024.12.013 |
| [45] | Xie XW, Jiang QM, Suo Y, et al. 0.23-Tesla MRI to differentiate between ischaemic and haemorrhagic strokes within 24 hours of onset: a combined experimental-clinical study[J]. Stroke Vasc Neurol, 2025, 10(4): 472-480. DOI:10.1136/svn-2024-003592 |
| [46] | Suo Y, Xie XW, Zhang Z, et al. 0.23 T MRI detects cerebral infarction in patients with minor ischemic stroke or TIA[J]. Stroke, 2024, 55(9): e249-e251. DOI:10.1161/STROKEAHA.124.047981 |
| [47] | Ringleb P, Bendszus M, Bluhmki E, et al. Extending the time window for intravenous thrombolysis in acute ischemic stroke using magnetic resonance imaging-based patient selection[J]. Int J Stroke, 2019, 14(5): 483-490. DOI:10.1177/1747493019840938 |
| [48] | Koga M, Yamamoto H, Inoue M, et al. Thrombolysis with alteplase at 0.6 mg/kg for stroke with unknown time of onset: a randomized controlled tria[J]. Stroke, 2020, 51(5): 1530-1538. DOI:10.1161/STROKEAHA.119.028127 |
| [49] | Luo ZY, Zhou Y, He YD, et al. Treatment with intravenous alteplase in ischaemic stroke patients with onset time between 4.5 and 24 hours (HOPE): protocol for a randomised, controlled, multicentre study[J]. Stroke Vasc Neurol, 2024, 9(3): 318-323. DOI:10.1136/svn-2022-002154 |
| [50] | Yan SQ, Zhou Y, Lansberg MG, et al. Alteplase for posterior circulation ischemic stroke at 4.5 to 24 hours[J]. N Engl J Med, 2025, 392(13): 1288-1296. DOI:10.1056/NEJMoa2413344 |
| [51] | Thomalla G, Boutitie F, Ma H, et al. Intravenous alteplase for stroke with unknown time of onset guided by advanced imaging: systematic review and meta-analysis of individual patient data[J]. Lancet, 2020, 396(10262): 1574-1584. DOI:10.1016/S0140-6736(20)32163-2 |
| [52] | Xiong YY, Campbell BCV, Schwamm LH, et al. Tenecteplase for ischemic stroke at 4.5 to 24 hours without thrombectomy[J]. N Engl J Med, 2024, 391(3): 203-212. DOI:10.1056/NEJMoa2402980 |
| [53] | Albers GW, Jumaa M, Purdon B, et al. Tenecteplase for stroke at 4.5 to 24 hours with perfusion-imaging selection[J]. N Engl J Med, 2024, 390(8): 701-711. DOI:10.1056/NEJMoa2310392 |
| [54] | Cheng X, Hong L, Lin LT, et al. Tenecteplase thrombolysis for stroke up to 24 hours after onset with perfusion imaging selection: the CHABLIS-T Ⅱ randomized clinical trial[J]. Stroke, 2025, 56(2): 344-354. DOI:10.1161/STROKEAHA.124.048375 |
| [55] | Yogendrakumar V, Campbell BC, Churilov L, et al. Extending the time window for tenecteplase by effective reperfusion of penumbral tissue in patients with large vessel occlusion: Rationale and design of a multicenter, prospective, randomized, open-label, blinded-endpoint, controlled phase 3 trial[J]. Int J Stroke, 2025, 20(3): 367-372. DOI:10.1177/17474930241308660 |
| [56] | Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American heart association/American stroke association[J]. Stroke, 2019, 50(12): e344-e418. DOI:10.1161/STR.0000000000000211DOI:10.1161/STR.0000000000000211 |
| [57] | Sarraj A, Mlynash M, Heit J, et al. Clinical outcomes and identification of patients with persistent penumbral profiles beyond 24 hours from last known well: analysis from DEFUSE 3[J]. Stroke, 2021, 52(3): 838-849. DOI:10.1161/STROKEAHA.120.031147 |
 2026, Vol. 35
2026, Vol. 35